Россия
Россия
Россия
Для определения зависимостей между входными переменными, технологическим режимом и выходными переменными процесса полимеризации этилена в автоклавном реакторе с мешалкой, а также анализа влияния конструктивных параметров реактора на эффективность требуется построение математической модели реактора полимеризации. Для решения этих задач предложена детерминированная математическая модель, полученная на основе анализа физико-химических закономерностей процесса полимеризации этилена. Приведены принципиальная схема полимеризации этилена с указанием потоков веществ и энергии, описание процесса, механизм химической кинетики полимеризации этилена, система допущений, упрощающих построение математической модели, уравнения математической модели реактора полимеризации этилена в автоклавном реакторе с мешалкой. Автоклавный реактор полимеризации этилена представлен как каскад аппаратов идеального смешения для описания каждой из зон реактора. Скорости химических реакций инициирования, роста и обрыва цепи выражены в соответствии с законом действующих масс. Математическая модель в окончательном виде представляет собой системы обыкновенных дифференциальных уравнений для описания каждой из зон реактора. Приведены исходные числовые значения переменных и параметров для моделирования процесса полимеризации этилена в автоклавном реакторе. Показаны результаты численных экспериментов, а также исследовано влияние различных факторов на выходные переменные процесса полимеризации этилена. Предложенная математическая модель может быть использована для оптимизации технологического режима процесса полимеризации этилена в автоклавном реакторе с мешалкой, а также для анализа влияния конструктивных параметров реактора на эффективность его работы.
полиэтилен, автоклавный реактор, математическая модель, реакция полимеризации, этилен, инициатор, температура в зоне реакции
Описание процесса
Технологический процесс полимеризации этилена осуществляется в автоклавном реакторе
с мешалкой. Реактор представляет собой цилиндрический аппарат с встроенным электроприводом мешалки. Объем реакционной зоны реактора составляет 0,25 м3. Реактор снабжен рубашкой, в которую подается охлаждающий воздух. Визуально реактор делится на 4 зоны. В каждую зону можно подавать различное количество этилена и инициатора, поддерживая в них разную температуру
и достигая разного среднего времени пребывания. Так, при давлении 150 МПа в первой зоне поддерживается температура 180 °С, образующийся при этом полимер имеет высокую молекулярную массу. В четвертой зоне устанавливается температура 280 °С и образуется полимер с низкой молекулярной массой. Смесь этих двух продуктов дает материал с нужными свойствами [1]. Схема полимеризации этилена в автоклавном реакторе с мешалкой представлена на рис. 1.
Этилен, компримированный до давления 150 МПа, поступает в реактор одновременно в двух местах ввода.
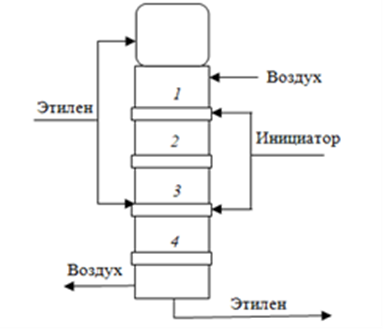
Рис. 1. Схема реактора полимеризации этилена:
1–4 – зоны автоклавного реактора
Fig. 1. Layout of the ethylene polymerization reactor:
1-4 – zones of the autoclave reactor
Первая половина этилена подается в 1-ю зону через корпус электродвигателя для его охлаждения, вторая половина – в зону 3 для создания и поддержания соответствующего температурного режима. Одновременно с этиленом в реактор вводится инициатор для инициирования реакции полимеризации этилена. Для подачи инициатора предусмотрено
2 ввода по высоте реактора – в зону 1 (верхний ввод) и зону 3 (нижний ввод).
Температура в реакторе регулируется изменением расхода инициатора в зависимости от применяемого инициатора и выпускаемой марки полиэтилена.
Выходящая из реактора реакционная смесь, состоящая из этилена и полиэтилена, поступает в холодильник.
В реакторе осуществляется процесс образования высокомолекулярного вещества (полимера) путем соединения большого числа молекул исходного низкомолекулярного вещества (мономера).
Для обеспечения работы реактора, в зависимости от марки выпускаемого полиэтилена, в реактор могут подаваться различные типы инициаторов:
– пероксид трет-бутила, эффективный в диапазоне 240–280 °C;
– трет-бутил пероксибензоат, эффективный в диапазоне 220–270 °C.
В целях обеспечения широкого спектра температур, необходимых для проведения реакции полимеризации, в реактор могут подаваться смеси инициаторов.
Процесс образования молекулы полимера состоит из следующих стадий:
а) инициирование для образования первичного свободного радикала:
![]() ;
;
б) рост цепи, заключающийся в последовательном присоединении к радикалу молекул мономера:
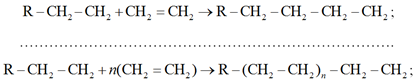
в) обрыв цепи, характеризующийся прекращением роста молекулы (взаимодействие растущих радикалов с образованием неактивных молекул полиэтилена рекомбинацией или диспропорционированием):
– рекомбинацией:
![]()
– диспропорционированием:
![]()
Если обозначить мономер (этилен) M, инициатор I, радикал (активную молекулу) X,
а полимер P, то реакцию полимеризации этилена можно представить:
– как инициирование:
![]() ;
;
– рост цепи:
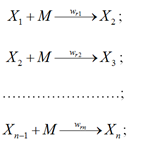
– обрыв цепи:
![]() ,
,
где стоящий при X индекс определяет степень полимеризации (длину цепи), а ![]() – скорости реакций инициирования, роста и обрыва цепи соответственно.
– скорости реакций инициирования, роста и обрыва цепи соответственно.
Система допущений
При образовании полимера, мольная масса которого велика, с достаточно хорошим приближением можно принять, что скорости реакций роста радикала, имеющего i-ю степень полимеризации ![]() , не зависят от степени полимеризации, т. е.
, не зависят от степени полимеризации, т. е. ![]() при любом i [2]. Это позволяет ввести суммарную концентрацию всех активных молекул как
при любом i [2]. Это позволяет ввести суммарную концентрацию всех активных молекул как ![]() и упростить схему реакций полимеризации этилена следующим образом:
и упростить схему реакций полимеризации этилена следующим образом:
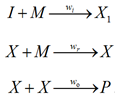 .
.
Через обозначены все радикалы, независимо от числа молекул мономера, входящих в состав радикалов, т. е. от степени полимеризации.
Так как количество молекул этилена, участвующих при инициировании в реакции с первичным радикалом, очень мало по сравнению с числом молекул этилена, участвующих в росте цепи (инициатор вводится в количестве до 1 % от массы этилена), примем допущение о том, что этилен расходуется только на полимеризацию [2].
4-х аппаратов идеального смешения для описания каждой из 4-х зон реактора. Схема потоков в зонах реактора показана на рис. 2.
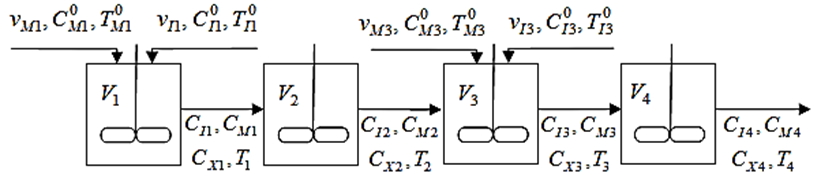

Математическое описание реактора
По закону действующих масс скорость химической реакции инициирования wi можно представить как
![]() ,
,
где ki – константа скорости инициирования; Ei – энергия активации реакции инициирования; R – универсальная газовая постоянная; T – абсолютная температура Кельвина; CM – концентрация этилена; CI – концентрация инициатора.
Скорость химической реакции роста цепи wr выражается уравнением
![]() , (1)
, (1)
где kr – константа скорости роста цепи; Er – энергия активации реакции роста цепи; CX – концентрация активных молекул.
Скорость химической реакции для обрыва цепи wo запишем как
![]() ,
,
где ko – константа скорости обрыва цепи; Eo – энергия активации реакции обрыва цепи.
Так как реактор проточный и на его входы подаются этилен и инициатор, то уравнения материального и теплового баланса по этим веществам можно представить в виде модели идеального смешения для непрерывного реактора.
Так, уравнение материального баланса по инициатору для 1-й зоны реактора можно представить в виде
![]() .
.
Уравнение материального баланса по этилену для 1-й зоны реактора с учетом того, что этилен расходуется только на реакцию полимеризации, можно представить в виде уравнения
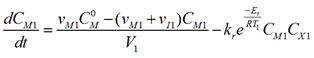 .
.
Уравнение материального баланса по радикалу выглядит следующим образом:
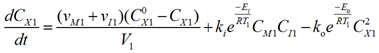 . (2)
. (2)
Примем допущение, что нет накопления радикалов в объеме реактора ![]() , т. е. все образующиеся радикалы расходуются на реакцию полимеризации (условие квазистационарности [2]), и поскольку нет радикалов во входных и выходном потоке, уравнение (2) примет вид
, т. е. все образующиеся радикалы расходуются на реакцию полимеризации (условие квазистационарности [2]), и поскольку нет радикалов во входных и выходном потоке, уравнение (2) примет вид
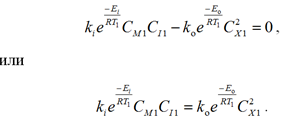
Отсюда можно выразить концентрацию радикалов
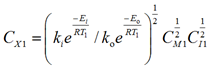 .
.
Тогда уравнение скорости химической реакции роста цепи (1) можно выразить уравнением
![]() , (3)
, (3)
где выражение ![]() есть константа скорости полимеризации
есть константа скорости полимеризации ![]() – суммарная энергия активации процесса полимеризации, которая находится как
– суммарная энергия активации процесса полимеризации, которая находится как
![]() .
.
С учетом выражения скорости реакции (3) материальный баланс по этилену примет вид
 .
.
Уравнение теплового баланса будет иметь вид
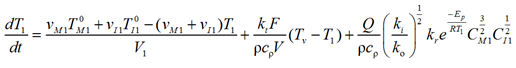 ,
,
где kt – коэффициент теплопередачи, Дж/(м2∙с∙°C); F – поверхность теплообмена, м2; ρ – плотность потока, кг/м3; cρ – удельная теплоемкость потока Дж/(кг∙°C); Тv – температура воздуха; Q – тепловой эффект реакции полимеризации, Дж/моль.
Окончательно математическая модель 1-й зоны реактора представляет собой систему из трех обыкновенных дифференциальных уравнений:
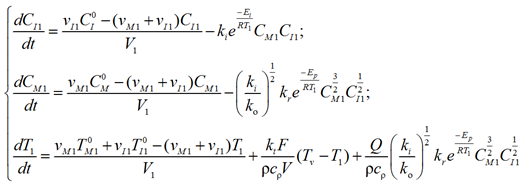 (4)
(4)
с начальными условиями
![]() (5)
(5)
и одного конечного уравнения
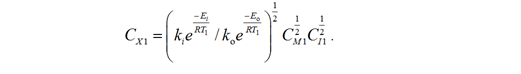 (6)
(6)
Аналогично записываются уравнения для остальных зон реактора:
– 2-я зона:
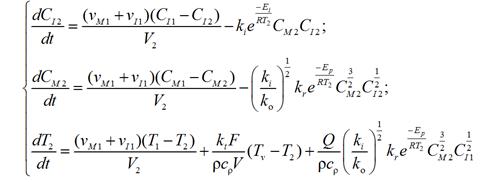 (7)
(7)
с начальными условиями
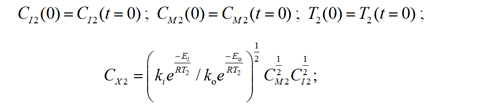
– 3-я зона:
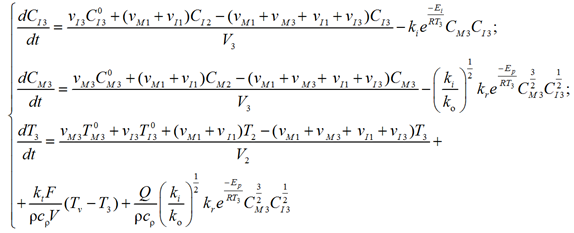 (10)
(10)
с начальными условиями
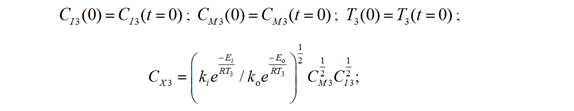
– 4-я зона:
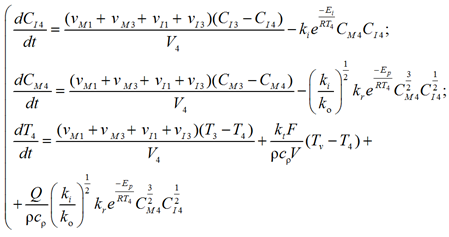 (13)
(13)
с начальными условиями
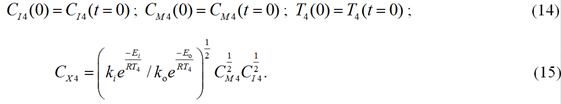
Математическая модель реактора полимеризации (4)–(15) содержит начальные условия (5), (8), (11) и (14), которые неизвестны и могут быть определены из решения уравнений модели статики. При расчете статического режима производные дифференциальных уравнений в модели приравниваются
к нулю и математическое описание переходит в систему конечных уравнений следующего вида:
– 1-я зона:
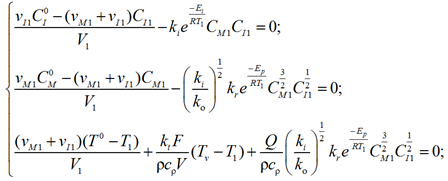 (16)
(16)
– 2-я зона:
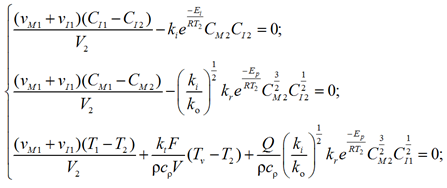 (17)
(17)
– 3-я зона:
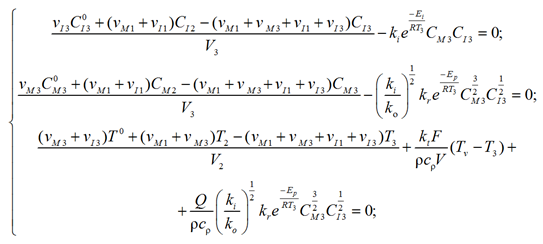 (18)
(18)
– 4-я зона:
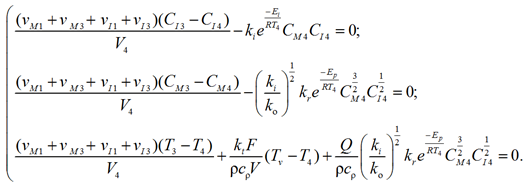 (19)
(19)
Получение решения уравнений модели не вызывает серьезных трудностей и может быть реализовано с помощью широко известных численных методов. Так, для решения системы нелинейных алгебраических уравнений (16)–(19) использовался метод Ньютона – Рафсона, а для решения систем дифференциальных уравнений (4), (7), (10), (13) метод Рунге – Кутта 4-го порядка.
В таблице приведены числовые данные при моделировании процесса полимеризации этилена в автоклавном реакторе с мешалкой.
Значения технологических переменных, констант и параметров, используемых в расчетах
Values of technological variables, constants and parameters used in the calculations
|
Переменная |
Значение |
Переменная |
Значение |
|
Объемные расходы этилена, м3/c |
0,0037 |
Константа инициирования, м3/кг∙с |
2 ∙ 1016 |
|
Концентрации этилена, кг/м3 |
445 |
Константа роста цепи, м3/кг∙с |
1 000 |
|
Объемные расходы инициатора, м3/c |
5,12 ∙ 10–4 |
Константа обрыва цепи, м3/кг∙с |
1 |
|
Концентрация инициатора, кг/м3 |
1,2 |
Энергия активации роста цепи, Дж/моль |
45 000 |
|
Температура этилена, К |
310 |
Энергия активации инициирования, Дж/моль |
180 000 |
|
Температура инициатора, К |
293 |
Энергия активации обрыва цепи, Дж/моль |
18 000 |
|
Объем зон реактора, м3 |
0,06 |
Универсальная постоянная, Дж/моль∙К |
8,31 |
|
Коэффициент теплопередачи, Дж/(м2∙с∙°C) |
5 |
Тепловой эффект полимеризации, Дж/моль |
96 000 |
|
Поверхность теплообмена, м2 |
15 |
Плотность потока, кг/м3 |
400 |
|
Температура воздуха, К |
293 |
Удельная теплоемкость потока, Дж/кг∙°C |
2 000 |
Были проведены численные эксперименты
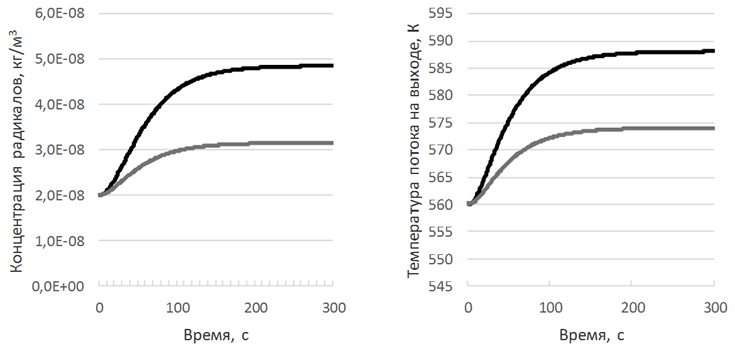
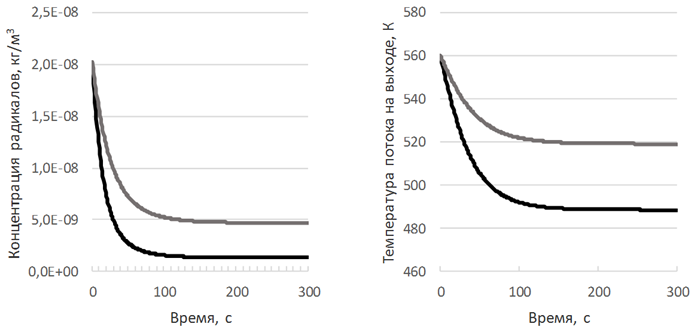
с помощью полученной модели, исследовано влияние различных факторов на выходные переменные процесса полимеризации этилена в автоклавном реакторе. На рис. 3 приведены отдельные результаты моделирования исследуемого процесса.
а
б
Рис. 3. Результаты моделирования реактора полимеризации при различных значениях входных переменных:
а – изменение концентрации радикалов и температуры с увеличением расхода инициатора
( на 5 % от номинального значения; на 10 % от номинального значения);
б – изменение концентрации радикалов и температуры с увеличением расхода этилена
( на 5 % от номинального значения; на 10 % от номинального значения)
Fig. 3. Simulation results of polymerization reactor at different values of input variables:
a – change of the radical concentration and temperature with increasing initiator flow rate
( by 5% of the nominal value; by 10% of the nominal value);
б – change of the radical concentration and temperature with increasing ethylene flow rate
( by 5% of the nominal value; by 10% of the nominal value)
Установлено, что с повышением расхода инициатора увеличивается концентрация активных молекул, растет скорость полимеризации. Так, например, увеличение расхода инициатора на 10 % от номинального значения ведет к росту температуры во всех зонах реакции в среднем на 30 °C
(см. рис. 3, а). Увеличение же расхода этилена на входе в реактор снижает температуру в зоне реакции и замедляет процесс полимеризации. Например, увеличение расхода этилена на 10 % от номинального значения ведет к снижению температуры на 70 °C (см. рис. 3, б).
Заключение
Исследовано влияние входной температуры, концентраций этилена и инициатора на входе в реактор. Так, повышение температуры этилена на входе увеличивает скорость реакции образования активных молекул, повышается температура в зоне реакции. Также на температуру в реакторе оказывает сильное влияние концентрация этилена на входе в реактор. С повышением концентрации этилена растет температура в реакторе.
Полученная математическая модель может быть использована для нахождения оптимального технологического режима процесса полимеризации этилена, а также для анализа влияния конструктивных параметров автоклавного реактора на эффективность его работы.
Исследовано влияние входной температуры, концентраций этилена и инициатора на входе в реактор. Так, повышение температуры этилена на входе увеличивает скорость реакции образования активных молекул, повышается температура в зоне реакции. Также на температуру в реакторе оказывает сильное влияние концентрация этилена на входе в реактор. С повышением концентрации этилена растет температура в реакторе.
Полученная математическая модель может быть использована для нахождения оптимального технологического режима процесса полимеризации этилена, а также для анализа влияния конструктивных параметров автоклавного реактора на эффективность его работы.
1. Технология полимерных материалов / под ред. В. К. Крыжановского. СПб.: ЦОП «Профессия», 2011. 536 с.
2. Вольтер Б. В., Сальников И. Е. Устойчивость режимов работы химических реакторов. М.: Химия, 1981. 200 с.















