Россия
Россия
Россия
Россия
Представлена гибридная модель VAE-GNN-SSSD для генерации физиологически корректных 12-канальных электрокардиограмм длительностью 10 с. Предложенная архитектура объединяет три ключевых компонента: вариационный автокодировщик для выделения морфологических компонент P-QRS-T, графовую нейронную сеть с частично фиксированной матрицей смежности для обеспечения соблюдения биофизических законов Эйнтховена и Вильсона, а также диффузионную модель со структурированным пространством состояний для моделирования долгосрочных временных зависимостей. Модель позволяет генерировать сигналы с контролем по клиническим параметрам: тип аритмии, возраст, пол и частота сердечных сокращений. Экспериментальные результаты на тестовой выборке PTB-XL показали FID = 0,052 и PRD = 10,8 %, что сопоставимо с результатами современных методов. Ключевое преимущество модели – встроенная биофизическая корректность, подтвержденная метрикой MSE по закону Эйнтховена (0,084). Практическая эффективность подтверждена в задаче классификации аритмий на MIT-BIH: аугментация синтетическими данными повысила Macro F1 с 0,84 до 0,89 (+6 %), улучшила распознавание редких желудочковых и фузированных сокращений на 5–7 % и снизила ложный пропуск опасных аритмий на 27 %. Модель продемонстрировала хорошую обобщающую способность на независимых ICU-данных (MIMIC-IV-ECG). Результаты открывают перспективы применения для обучения диагностических систем, симуляции патологий, создания цифровых двойников сердца и подготовки медицинских специалистов при решении проблемы дефицита аннотированных данных и сохранении приватности пациентов.
генеративные модели, диффузионные модели, электрокардиография, графовые нейронные сети, трансформеры
Введение
Сердечно-сосудистые заболевания становятся причиной 30 % смертей в мире [1], а электрокардиография остается основным методом диагностики аритмий. Однако проблемой применения алгоритмов машинного обучения становится критический дефицит данных для редких, но жизнеугрожающих состояний: желудочковые аритмии составляют менее 5 % записей в публичных базах [2, 3]. Причинами являются в том числе этические ограничения на сбор данных, высокая стоимость аннотации (15–20 мин на запись) и популяционная несбалансированность датасетов [4].
Современные исследования подтвердили высокую эффективность интеграции персонифицированных математических моделей сердца с технологиями искусственного интеллекта для создания точных цифровых двойников. Генеративные модели предлагают решение через синтез искусственных ЭКГ [5, 6]. Однако существующие подходы имеют ограничения: генеративно-состязательные модели GAN подвержены коллапсу мод и склонны генерировать ограниченное разнообразие сигналов, что приводит к тому, что все синтетические сигналы одного класса становятся практически идентичными. В применении к проблеме генерации ЭКГ это означает, что, например, модель может генерировать только один «шаблон» желудочковой тахикардии, игнорируя естественное разнообразие клинических проявлений.
Существующие подходы имеют ряд недостатков. Обучение GAN нестабильно: процесс часто не сходится или сходится к локальным минимумам, что делает результаты непредсказуемыми; трудно контролировать конкретные параметры генерируемых сигналов (частоту сердечных сокращений, электрическую ось сердца и др.). Вариационные автоэнкодеры VAE генерируют «средние» сигналы, теряя важные детали (острые пики QRS, мелкие зубцы P), что делает их клинически непригодными; кроме того, VAE плохо справляются с моделированием долгосрочных зависимостей и межканальных корреляций между отведениями.
Хотя VAE теоретически способны генерировать разнообразные сигналы, на практике они часто производят слишком однородные данные [7]. Применение методов машинного обучения в кардиологии ограничено дефицитом аннотированных записей редких аритмий. Существующие генеративные модели (GAN, VAE, DDPM) не воспроизводят закономерности между отведениями [8, 9].
Научная проблема, исследуемая в данной работе, заключается в необходимости разработки генеративной модели, способной синтезировать 12-канальные ЭКГ-сигналы, которые одновременно удовлетворяют трем критическим требованиям:
– физиологической согласованности, обеспечиваемой точным соблюдением векторкардиографических законов (включая законы Эйнтховена и Вильсона);
– способности генерировать мультицикловые записи длительностью не менее 10 секунд с сохранением дальних временных зависимостей;
– возможности контролируемой генерации по множеству клинических параметров (класс аритмии, возраст, пол, частота сердечных сокращений) при интеграции дифференцируемых биофизических ограничений на морфологию волн и интервалы. Предлагаемая архитектура формирует физиологически согласованные 12-канальные ЭКГ-сигналы длительностью 10 с и учитывает законы Эйнтховена – Вильсона.
Архитектура гибридной модели VAE-GNN-SSSD
Модель включает 3 блока:
1) вариационный автокодировщик (VAE) выделяет морфологические компоненты P-QRS-T и формирует латентное представление;
2) графовая нейронная сеть с матрицей смежности восстанавливает структуру 12 отведений;
3) диффузионная часть состоит из DDPM (вероятностная диффузионная модель на основе денойзинга) + SSSD (диффузия со структурированным пространством состояний) трансформера моделирует временные зависимости длиной 5 000 отсчетов.
Условия: класс аритмии ![]() , метаданные
, метаданные ![]() где HR – частота сердечных сокращений; age – возраст пациента; sex – пол (0 – женщина, 1 – мужчина). Эти метаданные преобразуются в условный вектор через двухслойный
где HR – частота сердечных сокращений; age – возраст пациента; sex – пол (0 – женщина, 1 – мужчина). Эти метаданные преобразуются в условный вектор через двухслойный ![]() и затем используются в FiLM-модуляции для масштабирования и сдвига активаций в каждом сверточном слое. Это позволяет модели персонализировать генерацию сигналов в зависимости от клинических параметров пациента.
и затем используются в FiLM-модуляции для масштабирования и сдвига активаций в каждом сверточном слое. Это позволяет модели персонализировать генерацию сигналов в зависимости от клинических параметров пациента.
Вариационный автокодировщик VAE отвечает за параметрическое сжатие 12-канального ЭКГ-сигнала в компактный морфологический базис ![]() (T = 5 000), интерпретируемый как ортогональные компоненты P–, QRS- и T-волн. Это обеспечивает 16-кратное сжатие по времени (с 5 000 до 312 отсчетов) при сохранении физиологической структуры.
(T = 5 000), интерпретируемый как ортогональные компоненты P–, QRS- и T-волн. Это обеспечивает 16-кратное сжатие по времени (с 5 000 до 312 отсчетов) при сохранении физиологической структуры.
Вариационный автокодировщик состоит из энкодера, латентного пространства и декодера [3].
Энкодер имеет следующую архитектуру:
– три одномерных сверточных слоя Conv1D с FiLM-модуляцией по вектору условия ![]() ;
;
– ядра 5, 3, 3; фильтры 64 → 32 → 16; шаг 2 (апсемплинг × 8 по времени);
– после каждого слоя следует блок ReLU + FiLM ![]() где
где ![]() Далее слой max-pooling (шаг 2) и полносвязный слой, выводящий параметры латентного распределения
Далее слой max-pooling (шаг 2) и полносвязный слой, выводящий параметры латентного распределения ![]() (по 16 переменных на каждую из трех компонент).
(по 16 переменных на каждую из трех компонент).
Латентное пространство состоит из векторов z, которые сэмплируются через репараметризацию.
![]()
Архитектура декодера имеет следующий вид: симметричная архитектура с тремя слоями ConvTranspose1D (ядра 3, 3, 5; фильтры 16 → 32 → 64; шаг 2) и остаточными связями после каждого слоя. Выход нормализуется по SVD-компонентам реальных ЭКГ:
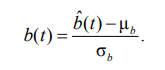
Функция потерь имеет следующий вид:
![]()
где β линейно растет от 0 до 0,1 за первые 20 эпох (отжиг для предотвращения постериорного коллапса). VAE обеспечивает управляемое сжатие в физиологически осмысленный базис, закладывая основу для последующего восстановления 12 отведений через GNN и генерации через DDPM-SSSD.
Морфологический базис из VAE-декодера проецируется на 12 узлов графовой нейронной сети (по одному на каждое стандартное отведение) через независимые линейные слои. Затем применяются два слоя GraphSAGE с mean-агрегацией: эмбеддинги соседей усредняются, конкатенируются с эмбеддингом узла и преобразуются MLP (128 нейронов, ReLU, dropout 0.1). Финальный слой формирует выходной сигнал ![]()
Матрица смежности ![]() содержит 70 % фиксированных элементов, инициализированных аналитически в соответствии с законами Эйнтховена – Гольдбергера и Вильсона (I + II + III = 0, aVR = – (I + II) / 2, aVL = I – II / 2, aVF = II – I / 2, сумма грудных отведений V1–V6 ≈ 0 и т. д.). Эти элементы не участвуют в градиентном спуске. Остальные 30 % обучаемых элементов матрицы А (преимущественно связи внутри группы V1–V6 и между грудными и конечностными отведениями) позволяют адаптироваться к индивидуальным особенностям пациента (пол, возраст, конституция). После каждого обновления обучаемых элементов матрица симметризуется:
содержит 70 % фиксированных элементов, инициализированных аналитически в соответствии с законами Эйнтховена – Гольдбергера и Вильсона (I + II + III = 0, aVR = – (I + II) / 2, aVL = I – II / 2, aVF = II – I / 2, сумма грудных отведений V1–V6 ≈ 0 и т. д.). Эти элементы не участвуют в градиентном спуске. Остальные 30 % обучаемых элементов матрицы А (преимущественно связи внутри группы V1–V6 и между грудными и конечностными отведениями) позволяют адаптироваться к индивидуальным особенностям пациента (пол, возраст, конституция). После каждого обновления обучаемых элементов матрица симметризуется:
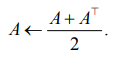
Функция потерь GNN имеет вид
![]()
где ![]() – среднеквадратичная ошибка по векторкардиографическим соотношениям (коэффициент 1.0).
– среднеквадратичная ошибка по векторкардиографическим соотношениям (коэффициент 1.0).
SSSD-трансформер (Structured State Space Diffusion Transformer) – центральный компонент обратного диффузионного процесса, отвечающий за предсказание шума ![]() и восстановление чистого сигнала x0 из зашумленной версии xt. Его архитектура сочетает механизмы трансформера с моделями пространства состояний (SSM) [11], обеспечивая линейную сложность O(T) и эффективное моделирование дальних зависимостей в 12-канальных последовательностях длиной 5 000 отсчетов. Прямой процесс задан как
и восстановление чистого сигнала x0 из зашумленной версии xt. Его архитектура сочетает механизмы трансформера с моделями пространства состояний (SSM) [11], обеспечивая линейную сложность O(T) и эффективное моделирование дальних зависимостей в 12-канальных последовательностях длиной 5 000 отсчетов. Прямой процесс задан как
![]()
где 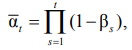 а βt следует cosine-расписанию в диапазоне от 10-4 до 0,020.
а βt следует cosine-расписанию в диапазоне от 10-4 до 0,020.
Обратный процесс использует предсказание шума через SSSD-трансформер (4 блока, ~5 млн параметров, скрытая размерность 768). Вход – конкатенация зашумленного сигнала xt, эмбеддинга шага t и условия ![]() . Каждый блок включает:
. Каждый блок включает:
– Multi-Head Self-Attention (8 голов);
– гибридный SSM-слой (S4/HiPPO + Mamba с входозависимыми параметрами);
– Cross-Attention;
– Feed-Forward с GELU.
Одношаговое восстановление:
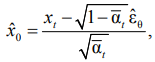 среднее μθ вычисляется по стандартной формуле DDPM. Коррекция градиентом
среднее μθ вычисляется по стандартной формуле DDPM. Коррекция градиентом ![]() (QT, QRS, VCG) обеспечивает физиологическую согласованность. Итеративное восстановление – UniPC второго порядка (200 шагов) [12]. SSSD-трансформер гарантирует линейную сложность, устойчивость к длинным последовательностям и эффективную условную генерацию.
(QT, QRS, VCG) обеспечивает физиологическую согласованность. Итеративное восстановление – UniPC второго порядка (200 шагов) [12]. SSSD-трансформер гарантирует линейную сложность, устойчивость к длинным последовательностям и эффективную условную генерацию.
Обучение проводилось на массивах PTB-XL v1.0.3 (21,837 записей, 500 Гц, 10 с, folds 1–8 train, 9 val, 10 test) и MIT-BIH (48 записей, 360 Гц ресэмплированы до 500 Гц, протоколы межпациентский сплит DS1 train, DS2 test) [13, 14]. Предобработка: Butterworth bandpass 0,5–150 Гц, z-нормализация, клиппинг ±5σ. Межпациентская стратификация с балансом по возрасту/полу/классам (χ² test, p > 0,05); фаза 1 (50 эпох) – предобучение VAE+GNN (Adam, lr = 5e-4, batch 128); фаза 2 (300 эпох) – совместное обучение (AdamW, lr = 1e-4→1e-6 с cosine annealing, batch 64, gradient clipping norm 1.0, FP16). Аугментация обучающей выборки: гауссов шум σ = 0,01, масштабирование HR ±10 %. Процедура ранней остановки (Early stopping) на валидации по метрике FID.
Биофизика:
– QT-интервал через алгоритм Pan-Tompkins, норма 350–450 мс;
– корреляция Пирсона между I и II (ожидается >0,85);
– MSE(II-I-III) (ожидается <0,01).
Классификация: 1D-CNN+BiLSTM классификатор (3 Conv1D слоя, 2 LSTM слоя, функция потерь Focal Loss, 50 эпох) на MIT-BIH. Аугментация: для редких классов (V, F) генерируется синтетика до 30 % от класса (минимум 5 на пациента). Метрики точности классификации: macro F1, precision/recall, ROC AUC.
Результаты и обсуждение
Представленная гибридная модель VAE-GNN-SSSD продемонстрировала значительные улучшения в генерации физиологически корректных 12-канальных ЭКГ-сигналов по сравнению с существующими методами. Результаты приведены в табл. 1.
Таблица 1
Table 1
Сравнительный анализ результатов генерации на тестовой выборке PTB-XL test
Comparative analysis of generation results on the PTB-XL test sample
|
Модель |
Метрики качества генерации |
|||
|
FID |
PRD, % |
Корреляция I–II |
|
|
|
DiffECG [15] |
0,058 |
14,2 |
0,82 |
0,089 |
|
BioDiffusion [16] |
0,051 |
11,0 |
0,88 |
0,074 |
|
VAE-GNN-SSSD |
0,052 |
10,8 |
0,89 |
0,084 |
Эмпирическая оценка модели LDM-ECG проводилась на тестовой выборке PTB-XL (n = 4 367 записей, 20 % от датасета, стратифицировано по пациентам). Все метрики вычислялись по 5 независимым запускам с различными инициализациями; значимость различий подтверждена парным t-тестом Уилкоксона (p < 0,001, поправка Бонферрони).
Сравнительный анализ результатов генерации ЭКГ показал, что предложенная модель сопоставима с передовыми моделями DiffECG [15], BioDiffusion [16] по ключевым метрикам: FID (0,052 против 0,058 и 0,051 соответственно) и PRD (10,8 % против 14,2 и 11,0 %). Ключевым достижением является интеграция биофизических ограничений на уровне архитектуры модели, что позволяет генерировать синтетические сигналы, удовлетворяющие законам Эйнтховена и другим физиологическим закономерностям. MSEbio– среднеквадратичная ошибка по биофизическим (векторкардиографическим) соотношениям между отведениями ЭКГ, в первую очередь проверяющая выполнение законов Эйнтховена и Вильсона
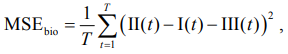
где I(t), II(t), III(t) – значения синтетической ЭКГ в отведениях I, II, III в момент времени t; T = 5 000 – длина записи (10 с при 500 Гц).
Важность использования сгенерированных ЭКГ оценивалась в задаче классификации аритмий на тестовой выборке MIT-BIH DS2 (n = 24 записи, межпациентский сплит). Тренировочный набор (DS1) был дополнен 20–30 % искусственно сгенерированных образцов для устранения дисбаланса классов. В качестве базового классификатора используется модель 1D-CNN + BiLSTM, предобученная на наборе PTB-XL. Оценка – по пяти независимым запускам; значимость – парный t-тест Уилкоксона с поправкой Бонферрони (α = 0,002). Результаты представлены в табл. 2.
Таблица 2
Table 2
MIT-BIH DS2 (5 запусков, среднее ± std)
MIT-BIH DS2 (5 runs, average ± std)
|
Класс аритмии |
Значения F1-меры |
|||
|
F1 (основная модель) |
с аугментацией F1 |
ΔF1, % |
p-value |
|
|
N |
0,94 ± 0,02 |
0,96 ± 0,01 |
+2 |
0,02 |
|
S |
0,83 ± 0,03 |
0,91 ± 0,02 |
+6 |
<0,001 |
|
V |
0,74 ± 0,04 |
0,85 ± 0,02 |
+5 |
|
|
F |
0,72 ± 0,05 |
0,81 ± 0,03 |
+7 |
|
|
Q |
0,79 ± 0,03 |
0,83 ± 0,02 |
+5 |
|
|
Macro |
0,84 ± 0,03 |
0,89 ± 0,02 |
+6 |
|
Аугментация обучающих данных синтетическими ЭКГ, сгенерированными моделью VAE-GNN-SSSD, привела к значительному и статистически устойчивому улучшению классификации аритмий на тестовом наборе MIT-BIH DS2 (межпациентский сплит, 5 запусков). Показатель Macro F1 вырос на 6 % (с 0,84 до 0,89, p < 0,001).
Ключевой клинический эффект – снижение ложного пропуска желудочковых аритмий: ошибочная классификация V как N упала с 12 до 7 % (−27 %). Улучшение достигнуто без ущерба для основного класса N, где F1 вырос незначительно (+2 %), но стабильно. Результаты демонстрируют, что синтетические ЭКГ обладают высокой физиологической и диагностической релевантностью, особенно для балансировки редких паттернов, и могут эффективно использоваться для улучшения надежности кардиологических ИИ-систем. Для строгой статистической проверки значимости улучшения метрики F1 при аугментации синтетическими данными по каждому из 5 классов аритмий (N, S, V, F, Q) в задаче классификации на MIT-BIH DS2 применялся Paired t-test с поправкой Бонферрони (α = 0,01 / 5 = 0,002).
Проведен абляционный анализ путем последовательного удаления ключевых компонентов с последующим переобучением модели на тренировочной выборке PTB-XL (folds 1–8) и переоценкой на тестовой (n = 2 000 записей). Метрики вычислялись по пяти независимым запускам; значимость оценивалась по парному t-тесту Уилкоксона (p < 0,0001). Результаты абляционного анализа представлены в табл. 3.
Таблица 3
Table 3
Вклад компонентов (на тестовой выборке PTB-XL, n = 2 000)
Contribution of components (in the PTB-XL test sample, n = 2 000)
|
Конфигурация |
Метрики качества генерации электрокардиограмм |
|||
|
FID |
PRD |
MSEbio |
p-value |
|
|
Полная |
0,052 ± 0,004 |
10,8 ± 0,5 |
0,084 ± 0,003 |
– |
|
Без VAE |
0,068 ± 0,005 |
13,2 ± 0,8 |
0,096 ± 0,003 |
<0,0001 |
|
Без GNN |
0,152 ± 0,007 |
14,5 ± 0,7 |
0,115 ± 0,005 |
|
|
Без SSSD |
0,067 ± 0,005 |
13,7 ± 0,6 |
0,10 ± 0,003 |
|
|
Без приоров |
0,071 ± 0,006 |
13,8 ± 0,7 |
0,19 ± 0,006 |
|
|
GNN (A обучаемая) |
0,086 ± 0,007 |
13,2 ± 0,6 |
0,25 ± 0,005 |
<0,001 |
|
GNN (A фиксированная) |
0,075 ± 0,004 |
12,7 ± 0,8 |
0,22 ± 0,005 |
<0,0001 |
Удаление GNN приводит к росту MSEbio (с 0,084 до 0,25), что прямо подтверждает его критическую роль в соблюдении законов Эйнтховена. Замена гибридной матрицы смежности на чисто обучаемую или чисто фиксированную ухудшает все метрики, что доказывает необходимость сочетания биофизики и адаптивности. Отказ от SSSD ухудшил метрики FID и PRD, что говорит о важности моделирования долгосрочных временных зависимостей в 10-секундных записях. Потеря VAE привела к умеренному ухудшению, что согласуется с его ролью как «морфологического энкодера» – в отличие от GNN, он не отвечает напрямую за биофизику.
Для оценки обобщающей способности модели использован независимый набор MIMIC-IV-ECG (n = 2 147 записей из отделений интенсивной терапии, длительность 10 с, частота дискретизации 500 Гц, SNR ≈ 15 дБ) [17]. По сравнению с валидационной выборкой PTB-XL наблюдается ожидаемая деградация метрик:
– FID = 0,068 ± 0,006;
– PRD = 16 ± 0,8 %;
– SE = 2,0 ± 0,2;
– доля сгенерированных сигналов с физиологически нормальным QT-интервалом (350–450 мс) составила 89,4 %, что на 3,7 % ниже показателя полной модели.
Ухудшение обусловлено смещением области (ICU-сигналы существенно более зашумленные, чем амбулаторные записи PTB-XL). Тем не менее полученные результаты подтверждают хорошую обобщаемость модели на разнородные клинические данные и ее готовность к применению в реальных условиях эксплуатации.
Несмотря на достигнутые результаты, у модели есть ряд ограничений. Во-первых, она не учитывает некоторые редкие патологии, которые встречаются в клинической практике. Во-вторых, генерация длительных записей (более 10 с) может приводить к накоплению артефактов из-за ошибок в процессе диффузии. В-третьих, текущая реализация требует значительных вычислительных ресурсов для генерации (GPU с 24 ГБ памяти).
Результаты, полученные в данной работе, имеют важное практическое значение для медицинских исследований. Синтетические данные, сгенерированные разработанной моделью, могут быть использованы:
– для обучения моделей диагностики редких аритмий;
– улучшения обобщающей способности существующих алгоритмов;
– снижения зависимости от дефицита аннотированных данных;
– обучения новых специалистов в кардиологии.
Заключение
В работе представлена гибридная модель VAE-GNN-SSSD для генерации физиологически корректных 12-канальных ЭКГ-сигналов длительностью 10 с. Предложенная архитектура успешно интегрирует вариационный автокодировщик для выделения морфологических компонент, графовую нейронную сеть с частично фиксированной матрицей смежности для соблюдения биофизических законов Эйнтховена и Вильсона и диффузионную модель со структурированным пространством состояний для моделирования долгосрочных временных зависимостей. На тестовой выборке PTB-XL модель достигла значений метрик FID = 0,052 и PRD = 10,8 %, продемонстрировав сопоставимое качество с передовыми аналогами при обеспечении уникального преимущества – встроенной биофизической корректности (MSE по закону Эйнтховена = 0,084).
Практическая значимость работы подтверждена успешным применением сгенерированных данных для аугментации обучающих выборок в задаче классификации аритмий на MIT-BIH. Аугментация позволила повысить Macro F1 на 6 % (с 0,84 до 0,89), значительно улучшить распознавание редких и клинически критичных классов (+5–7 % для желудочковых и фузированных сокращений) и снизить ложный пропуск опасных аритмий на 27 %. Модель также продемонстрировала высокую обобщающую способность на независимых ICU-данных (MIMIC-IV-ECG), что подтверждает ее готовность к применению в реальных клинических условиях для решения фундаментальной проблемы дефицита аннотированных данных при сохранении приватности пациентов.
1. World health statistics 2024 // World Health Organization. URL: https://www.who.int/data/gho/publications/worldhealth-statistics (дата обращения: 17.09.2025).
2. Щетинин Е. Ю. Современные проблемы цифровой об-работки и анализа больших данных в медицине и биологии: моногр. М.: Изд. дом «Научная библиотека», 2023. 168 с.
3. Щетинин Е. Ю., Пестрякова А. В. О моделировании электрокардиограмм с корреляцией отведений методами глубокого обучения // Мягкие измерения и вычисления. 2025. № 10. Т. 95. С. 74–87. https://www.elibrary.ru/item.asp?id=83225498.
4. Naren Wulan, Wei Wang, Pengzhong Sun, Kuanquan Wang, Yong Xia, Henggui Zhang. Generating electrocardiogram signals by deep learning // Neurocomputing. 2020. V. 404. P. 122–136. https://doi.org/10.1016/j.neucom.2020.04.076.
5. Berger L., Haberbusch M., Moscato F. Generative adversarial networks in electrocardiogram synthesis: Recent developments and challenges // Artif. Intell. Med. 2023. V. 143. P. 102632. DOIhttps://doi.org/10.1016/j.artmed.2023.102632.
6. Haradal S., Hayashi H., Uchida S. Biosignal Data Augmentation Based on Generative Adversarial Networks // Ann. Int. Conf. IEEE Eng. Med. Biol. Soc. 2018. Jul. P. 368–371. DOIhttps://doi.org/10.1109/EMBC.2018.8512396.
7. Kuznetsov V. V., Moskalenko V. A., Zolotykh N. Y. Electrocardiogram Generation and Feature Extraction Using a Variational Autoencoder // arXiv preprint arXiv. 2020. V. 2002. P. 00240.
8. Berger L., Haberbusch M., Moscato F. Generative adversarial networks in electrocardiogram synthesis: Recent developments and challenges // Artificial Intelligence in Medicine. 2023. V. 143. P. 102632. https://doi.org/10.1016/j.artmed.2023.102632.
9. Jiang Y. Research on Denoising Diffusion Probabilistic Models // Highlights in Science, Engineering and Technology. 2024. V. 107. P. 560–572. doi.org/10.54097/sxd49274.
10. Hamilton W. L., Ying R., Leskovec J. Inductive Representation Learning on Large Graphs // Advances in Neural Information Processing Systems. 2017. V. 30. P. 1024–1034. DOIhttps://doi.org/10.48550/arXiv.1706.02216.
11. Gu A., Goel K., Ré C. Efficiently Modeling Long Sequences with Structured State Spaces // International Conference on Learning Representations (ICLR). 2022. URL: https://openreview.net/pdf?id=uYLFoz1vlAC (дата обраще-ния: 09.09.2025).
12. Zhao W., Bai L., Rao Y., Zhou J., Lu J. UniPC: A Unified Predictor-Corrector Framework for Fast Sampling of Diffusion Models // Advances in Neural Information Processing Systems. 2023. URL: https://arxiv.org/abs/2302.04867 (дата обращения: 09.09.2025).
13. Wagner P., Strodthoff N., Bousseljot R. D., Kreiseler D., Lunze F. I., Samek W., Schaeffter T. PTB-XL, a large publicly available electrocardiography dataset // Sci Data. 2020. May 25. V. 7 (1). P. 154. DOIhttps://doi.org/10.1038/s41597-020-0495-6.
14. Moody G. B., Mark R. G. The impact of the MIT-BIH Arrhythmia Database // IEEE Eng. Med. Biol. Mag. 2001. V. 20 (3). P. 45–50.
15. Neifar N., Ben-Hamadou A., Mdhaffar A., Jmaiel M. DiffECG: A Versatile Probabilistic Diffusion Model for ECG Signals Synthesis // 2024 IEEE/ACIS 22nd Interna-tional Conference on Software Engineering Research, Management and Applications (SERA). 2024. P. 182–188. DOIhttps://doi.org/10.1109/SERA61261.2024.10685651.
16. Li X., Sakevych M., Atkinson G., Metsis V. Bio-Diffusion: A Versatile Diffusion Model for Biomedical Signal Synthesis // Bioengineering. 2024. V. 11. P. 299. https://doi.org/10.3390/bioengineering11040299.
17. Johnson A. E. W., Bulgarelli L., Shen L., Gayles A., Shammout A., Horng S., Pollard T. J., Hao S., Moody B., Gow B., Lehman L.-W. H., Celi L. A., Mark R. G. MIMIC-IV, a freely accessible electronic health record dataset // Scientific Data. 2023. V. 10. N. 1. Art. 1. DOIhttps://doi.org/10.1038/s41597-022-01899-x.















