Russian Federation
Russian Federation
Russian Federation
Russian Federation
A hybrid VAE-GNN-SSSD model is presented for generating physiologically correct 12-channel electro-cardiograms with a duration of 10 seconds. The proposed architecture combines three key components: a variational autoencoder for isolating the morphological components of P-QRS-T, a graph neural network with a partially fixed adjacency matrix to ensure compliance with the biophysical laws of Einthoven and Wilson, as well as a diffusion model with a structured state space for modeling long-term time dependencies. The model allows you to generate signals controlled by clinical parameters: type of arrhythmia, age, gender, and heart rate. Experimental results on the PTB-XL test sample showed FID = 0.052 and PRD = 10.8%, which is comparable with the results of modern methods. The key advantage of the model is its built–in biophysical correctness, confirmed by the MSE metric according to Einthoven's law (0.084). The practical effectiveness was confirmed in the MIT BIH classification of arrhythmias: augmentation with synthetic data increased Macro F1 from 0.84 to 0.89 (+6%), improved the recognition of rare ventricular and fuzed contractions by 5-7% and reduced the false omission of dangerous arrhythmias by 27%. The model has demonstrated good generalizing ability on independent ICU data (MIMIC-IV-ECG). The results open up prospects for the use of diagnostic systems for training, pathology simulation, creation of digital heart twins and training of medical specialists in solving the problem of shortage of annotated data and maintaining patient privacy.
generative models, diffusion models, electrocardiography, graph neural networks, transformers
Введение
Сердечно-сосудистые заболевания становятся причиной 30 % смертей в мире [1], а электрокардиография остается основным методом диагностики аритмий. Однако проблемой применения алгоритмов машинного обучения становится критический дефицит данных для редких, но жизнеугрожающих состояний: желудочковые аритмии составляют менее 5 % записей в публичных базах [2, 3]. Причинами являются в том числе этические ограничения на сбор данных, высокая стоимость аннотации (15–20 мин на запись) и популяционная несбалансированность датасетов [4].
Современные исследования подтвердили высокую эффективность интеграции персонифицированных математических моделей сердца с технологиями искусственного интеллекта для создания точных цифровых двойников. Генеративные модели предлагают решение через синтез искусственных ЭКГ [5, 6]. Однако существующие подходы имеют ограничения: генеративно-состязательные модели GAN подвержены коллапсу мод и склонны генерировать ограниченное разнообразие сигналов, что приводит к тому, что все синтетические сигналы одного класса становятся практически идентичными. В применении к проблеме генерации ЭКГ это означает, что, например, модель может генерировать только один «шаблон» желудочковой тахикардии, игнорируя естественное разнообразие клинических проявлений.
Существующие подходы имеют ряд недостатков. Обучение GAN нестабильно: процесс часто не сходится или сходится к локальным минимумам, что делает результаты непредсказуемыми; трудно контролировать конкретные параметры генерируемых сигналов (частоту сердечных сокращений, электрическую ось сердца и др.). Вариационные автоэнкодеры VAE генерируют «средние» сигналы, теряя важные детали (острые пики QRS, мелкие зубцы P), что делает их клинически непригодными; кроме того, VAE плохо справляются с моделированием долгосрочных зависимостей и межканальных корреляций между отведениями.
Хотя VAE теоретически способны генерировать разнообразные сигналы, на практике они часто производят слишком однородные данные [7]. Применение методов машинного обучения в кардиологии ограничено дефицитом аннотированных записей редких аритмий. Существующие генеративные модели (GAN, VAE, DDPM) не воспроизводят закономерности между отведениями [8, 9].
Научная проблема, исследуемая в данной работе, заключается в необходимости разработки генеративной модели, способной синтезировать 12-канальные ЭКГ-сигналы, которые одновременно удовлетворяют трем критическим требованиям:
– физиологической согласованности, обеспечиваемой точным соблюдением векторкардиографических законов (включая законы Эйнтховена и Вильсона);
– способности генерировать мультицикловые записи длительностью не менее 10 секунд с сохранением дальних временных зависимостей;
– возможности контролируемой генерации по множеству клинических параметров (класс аритмии, возраст, пол, частота сердечных сокращений) при интеграции дифференцируемых биофизических ограничений на морфологию волн и интервалы. Предлагаемая архитектура формирует физиологически согласованные 12-канальные ЭКГ-сигналы длительностью 10 с и учитывает законы Эйнтховена – Вильсона.
Архитектура гибридной модели VAE-GNN-SSSD
Модель включает 3 блока:
1) вариационный автокодировщик (VAE) выделяет морфологические компоненты P-QRS-T и формирует латентное представление;
2) графовая нейронная сеть с матрицей смежности восстанавливает структуру 12 отведений;
3) диффузионная часть состоит из DDPM (вероятностная диффузионная модель на основе денойзинга) + SSSD (диффузия со структурированным пространством состояний) трансформера моделирует временные зависимости длиной 5 000 отсчетов.
Условия: класс аритмии ![]() , метаданные
, метаданные ![]() где HR – частота сердечных сокращений; age – возраст пациента; sex – пол (0 – женщина, 1 – мужчина). Эти метаданные преобразуются в условный вектор через двухслойный
где HR – частота сердечных сокращений; age – возраст пациента; sex – пол (0 – женщина, 1 – мужчина). Эти метаданные преобразуются в условный вектор через двухслойный ![]() и затем используются в FiLM-модуляции для масштабирования и сдвига активаций в каждом сверточном слое. Это позволяет модели персонализировать генерацию сигналов в зависимости от клинических параметров пациента.
и затем используются в FiLM-модуляции для масштабирования и сдвига активаций в каждом сверточном слое. Это позволяет модели персонализировать генерацию сигналов в зависимости от клинических параметров пациента.
Вариационный автокодировщик VAE отвечает за параметрическое сжатие 12-канального ЭКГ-сигнала в компактный морфологический базис ![]() (T = 5 000), интерпретируемый как ортогональные компоненты P–, QRS- и T-волн. Это обеспечивает 16-кратное сжатие по времени (с 5 000 до 312 отсчетов) при сохранении физиологической структуры.
(T = 5 000), интерпретируемый как ортогональные компоненты P–, QRS- и T-волн. Это обеспечивает 16-кратное сжатие по времени (с 5 000 до 312 отсчетов) при сохранении физиологической структуры.
Вариационный автокодировщик состоит из энкодера, латентного пространства и декодера [3].
Энкодер имеет следующую архитектуру:
– три одномерных сверточных слоя Conv1D с FiLM-модуляцией по вектору условия ![]() ;
;
– ядра 5, 3, 3; фильтры 64 → 32 → 16; шаг 2 (апсемплинг × 8 по времени);
– после каждого слоя следует блок ReLU + FiLM ![]() где
где ![]() Далее слой max-pooling (шаг 2) и полносвязный слой, выводящий параметры латентного распределения
Далее слой max-pooling (шаг 2) и полносвязный слой, выводящий параметры латентного распределения ![]() (по 16 переменных на каждую из трех компонент).
(по 16 переменных на каждую из трех компонент).
Латентное пространство состоит из векторов z, которые сэмплируются через репараметризацию.
![]()
Архитектура декодера имеет следующий вид: симметричная архитектура с тремя слоями ConvTranspose1D (ядра 3, 3, 5; фильтры 16 → 32 → 64; шаг 2) и остаточными связями после каждого слоя. Выход нормализуется по SVD-компонентам реальных ЭКГ:
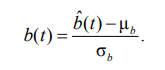
Функция потерь имеет следующий вид:
![]()
где β линейно растет от 0 до 0,1 за первые 20 эпох (отжиг для предотвращения постериорного коллапса). VAE обеспечивает управляемое сжатие в физиологически осмысленный базис, закладывая основу для последующего восстановления 12 отведений через GNN и генерации через DDPM-SSSD.
Морфологический базис из VAE-декодера проецируется на 12 узлов графовой нейронной сети (по одному на каждое стандартное отведение) через независимые линейные слои. Затем применяются два слоя GraphSAGE с mean-агрегацией: эмбеддинги соседей усредняются, конкатенируются с эмбеддингом узла и преобразуются MLP (128 нейронов, ReLU, dropout 0.1). Финальный слой формирует выходной сигнал ![]()
Матрица смежности ![]() содержит 70 % фиксированных элементов, инициализированных аналитически в соответствии с законами Эйнтховена – Гольдбергера и Вильсона (I + II + III = 0, aVR = – (I + II) / 2, aVL = I – II / 2, aVF = II – I / 2, сумма грудных отведений V1–V6 ≈ 0 и т. д.). Эти элементы не участвуют в градиентном спуске. Остальные 30 % обучаемых элементов матрицы А (преимущественно связи внутри группы V1–V6 и между грудными и конечностными отведениями) позволяют адаптироваться к индивидуальным особенностям пациента (пол, возраст, конституция). После каждого обновления обучаемых элементов матрица симметризуется:
содержит 70 % фиксированных элементов, инициализированных аналитически в соответствии с законами Эйнтховена – Гольдбергера и Вильсона (I + II + III = 0, aVR = – (I + II) / 2, aVL = I – II / 2, aVF = II – I / 2, сумма грудных отведений V1–V6 ≈ 0 и т. д.). Эти элементы не участвуют в градиентном спуске. Остальные 30 % обучаемых элементов матрицы А (преимущественно связи внутри группы V1–V6 и между грудными и конечностными отведениями) позволяют адаптироваться к индивидуальным особенностям пациента (пол, возраст, конституция). После каждого обновления обучаемых элементов матрица симметризуется:
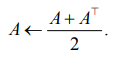
Функция потерь GNN имеет вид
![]()
где ![]() – среднеквадратичная ошибка по векторкардиографическим соотношениям (коэффициент 1.0).
– среднеквадратичная ошибка по векторкардиографическим соотношениям (коэффициент 1.0).
SSSD-трансформер (Structured State Space Diffusion Transformer) – центральный компонент обратного диффузионного процесса, отвечающий за предсказание шума ![]() и восстановление чистого сигнала x0 из зашумленной версии xt. Его архитектура сочетает механизмы трансформера с моделями пространства состояний (SSM) [11], обеспечивая линейную сложность O(T) и эффективное моделирование дальних зависимостей в 12-канальных последовательностях длиной 5 000 отсчетов. Прямой процесс задан как
и восстановление чистого сигнала x0 из зашумленной версии xt. Его архитектура сочетает механизмы трансформера с моделями пространства состояний (SSM) [11], обеспечивая линейную сложность O(T) и эффективное моделирование дальних зависимостей в 12-канальных последовательностях длиной 5 000 отсчетов. Прямой процесс задан как
![]()
где 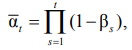 а βt следует cosine-расписанию в диапазоне от 10-4 до 0,020.
а βt следует cosine-расписанию в диапазоне от 10-4 до 0,020.
Обратный процесс использует предсказание шума через SSSD-трансформер (4 блока, ~5 млн параметров, скрытая размерность 768). Вход – конкатенация зашумленного сигнала xt, эмбеддинга шага t и условия ![]() . Каждый блок включает:
. Каждый блок включает:
– Multi-Head Self-Attention (8 голов);
– гибридный SSM-слой (S4/HiPPO + Mamba с входозависимыми параметрами);
– Cross-Attention;
– Feed-Forward с GELU.
Одношаговое восстановление:
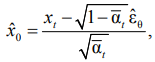 среднее μθ вычисляется по стандартной формуле DDPM. Коррекция градиентом
среднее μθ вычисляется по стандартной формуле DDPM. Коррекция градиентом ![]() (QT, QRS, VCG) обеспечивает физиологическую согласованность. Итеративное восстановление – UniPC второго порядка (200 шагов) [12]. SSSD-трансформер гарантирует линейную сложность, устойчивость к длинным последовательностям и эффективную условную генерацию.
(QT, QRS, VCG) обеспечивает физиологическую согласованность. Итеративное восстановление – UniPC второго порядка (200 шагов) [12]. SSSD-трансформер гарантирует линейную сложность, устойчивость к длинным последовательностям и эффективную условную генерацию.
Обучение проводилось на массивах PTB-XL v1.0.3 (21,837 записей, 500 Гц, 10 с, folds 1–8 train, 9 val, 10 test) и MIT-BIH (48 записей, 360 Гц ресэмплированы до 500 Гц, протоколы межпациентский сплит DS1 train, DS2 test) [13, 14]. Предобработка: Butterworth bandpass 0,5–150 Гц, z-нормализация, клиппинг ±5σ. Межпациентская стратификация с балансом по возрасту/полу/классам (χ² test, p > 0,05); фаза 1 (50 эпох) – предобучение VAE+GNN (Adam, lr = 5e-4, batch 128); фаза 2 (300 эпох) – совместное обучение (AdamW, lr = 1e-4→1e-6 с cosine annealing, batch 64, gradient clipping norm 1.0, FP16). Аугментация обучающей выборки: гауссов шум σ = 0,01, масштабирование HR ±10 %. Процедура ранней остановки (Early stopping) на валидации по метрике FID.
Биофизика:
– QT-интервал через алгоритм Pan-Tompkins, норма 350–450 мс;
– корреляция Пирсона между I и II (ожидается >0,85);
– MSE(II-I-III) (ожидается <0,01).
Классификация: 1D-CNN+BiLSTM классификатор (3 Conv1D слоя, 2 LSTM слоя, функция потерь Focal Loss, 50 эпох) на MIT-BIH. Аугментация: для редких классов (V, F) генерируется синтетика до 30 % от класса (минимум 5 на пациента). Метрики точности классификации: macro F1, precision/recall, ROC AUC.
Результаты и обсуждение
Представленная гибридная модель VAE-GNN-SSSD продемонстрировала значительные улучшения в генерации физиологически корректных 12-канальных ЭКГ-сигналов по сравнению с существующими методами. Результаты приведены в табл. 1.
Таблица 1
Table 1
Сравнительный анализ результатов генерации на тестовой выборке PTB-XL test
Comparative analysis of generation results on the PTB-XL test sample
|
Модель |
Метрики качества генерации |
|||
|
FID |
PRD, % |
Корреляция I–II |
|
|
|
DiffECG [15] |
0,058 |
14,2 |
0,82 |
0,089 |
|
BioDiffusion [16] |
0,051 |
11,0 |
0,88 |
0,074 |
|
VAE-GNN-SSSD |
0,052 |
10,8 |
0,89 |
0,084 |
Эмпирическая оценка модели LDM-ECG проводилась на тестовой выборке PTB-XL (n = 4 367 записей, 20 % от датасета, стратифицировано по пациентам). Все метрики вычислялись по 5 независимым запускам с различными инициализациями; значимость различий подтверждена парным t-тестом Уилкоксона (p < 0,001, поправка Бонферрони).
Сравнительный анализ результатов генерации ЭКГ показал, что предложенная модель сопоставима с передовыми моделями DiffECG [15], BioDiffusion [16] по ключевым метрикам: FID (0,052 против 0,058 и 0,051 соответственно) и PRD (10,8 % против 14,2 и 11,0 %). Ключевым достижением является интеграция биофизических ограничений на уровне архитектуры модели, что позволяет генерировать синтетические сигналы, удовлетворяющие законам Эйнтховена и другим физиологическим закономерностям. MSEbio– среднеквадратичная ошибка по биофизическим (векторкардиографическим) соотношениям между отведениями ЭКГ, в первую очередь проверяющая выполнение законов Эйнтховена и Вильсона
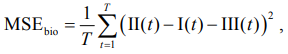
где I(t), II(t), III(t) – значения синтетической ЭКГ в отведениях I, II, III в момент времени t; T = 5 000 – длина записи (10 с при 500 Гц).
Важность использования сгенерированных ЭКГ оценивалась в задаче классификации аритмий на тестовой выборке MIT-BIH DS2 (n = 24 записи, межпациентский сплит). Тренировочный набор (DS1) был дополнен 20–30 % искусственно сгенерированных образцов для устранения дисбаланса классов. В качестве базового классификатора используется модель 1D-CNN + BiLSTM, предобученная на наборе PTB-XL. Оценка – по пяти независимым запускам; значимость – парный t-тест Уилкоксона с поправкой Бонферрони (α = 0,002). Результаты представлены в табл. 2.
Таблица 2
Table 2
MIT-BIH DS2 (5 запусков, среднее ± std)
MIT-BIH DS2 (5 runs, average ± std)
|
Класс аритмии |
Значения F1-меры |
|||
|
F1 (основная модель) |
с аугментацией F1 |
ΔF1, % |
p-value |
|
|
N |
0,94 ± 0,02 |
0,96 ± 0,01 |
+2 |
0,02 |
|
S |
0,83 ± 0,03 |
0,91 ± 0,02 |
+6 |
<0,001 |
|
V |
0,74 ± 0,04 |
0,85 ± 0,02 |
+5 |
|
|
F |
0,72 ± 0,05 |
0,81 ± 0,03 |
+7 |
|
|
Q |
0,79 ± 0,03 |
0,83 ± 0,02 |
+5 |
|
|
Macro |
0,84 ± 0,03 |
0,89 ± 0,02 |
+6 |
|
Аугментация обучающих данных синтетическими ЭКГ, сгенерированными моделью VAE-GNN-SSSD, привела к значительному и статистически устойчивому улучшению классификации аритмий на тестовом наборе MIT-BIH DS2 (межпациентский сплит, 5 запусков). Показатель Macro F1 вырос на 6 % (с 0,84 до 0,89, p < 0,001).
Ключевой клинический эффект – снижение ложного пропуска желудочковых аритмий: ошибочная классификация V как N упала с 12 до 7 % (−27 %). Улучшение достигнуто без ущерба для основного класса N, где F1 вырос незначительно (+2 %), но стабильно. Результаты демонстрируют, что синтетические ЭКГ обладают высокой физиологической и диагностической релевантностью, особенно для балансировки редких паттернов, и могут эффективно использоваться для улучшения надежности кардиологических ИИ-систем. Для строгой статистической проверки значимости улучшения метрики F1 при аугментации синтетическими данными по каждому из 5 классов аритмий (N, S, V, F, Q) в задаче классификации на MIT-BIH DS2 применялся Paired t-test с поправкой Бонферрони (α = 0,01 / 5 = 0,002).
Проведен абляционный анализ путем последовательного удаления ключевых компонентов с последующим переобучением модели на тренировочной выборке PTB-XL (folds 1–8) и переоценкой на тестовой (n = 2 000 записей). Метрики вычислялись по пяти независимым запускам; значимость оценивалась по парному t-тесту Уилкоксона (p < 0,0001). Результаты абляционного анализа представлены в табл. 3.
Таблица 3
Table 3
Вклад компонентов (на тестовой выборке PTB-XL, n = 2 000)
Contribution of components (in the PTB-XL test sample, n = 2 000)
|
Конфигурация |
Метрики качества генерации электрокардиограмм |
|||
|
FID |
PRD |
MSEbio |
p-value |
|
|
Полная |
0,052 ± 0,004 |
10,8 ± 0,5 |
0,084 ± 0,003 |
– |
|
Без VAE |
0,068 ± 0,005 |
13,2 ± 0,8 |
0,096 ± 0,003 |
<0,0001 |
|
Без GNN |
0,152 ± 0,007 |
14,5 ± 0,7 |
0,115 ± 0,005 |
|
|
Без SSSD |
0,067 ± 0,005 |
13,7 ± 0,6 |
0,10 ± 0,003 |
|
|
Без приоров |
0,071 ± 0,006 |
13,8 ± 0,7 |
0,19 ± 0,006 |
|
|
GNN (A обучаемая) |
0,086 ± 0,007 |
13,2 ± 0,6 |
0,25 ± 0,005 |
<0,001 |
|
GNN (A фиксированная) |
0,075 ± 0,004 |
12,7 ± 0,8 |
0,22 ± 0,005 |
<0,0001 |
Удаление GNN приводит к росту MSEbio (с 0,084 до 0,25), что прямо подтверждает его критическую роль в соблюдении законов Эйнтховена. Замена гибридной матрицы смежности на чисто обучаемую или чисто фиксированную ухудшает все метрики, что доказывает необходимость сочетания биофизики и адаптивности. Отказ от SSSD ухудшил метрики FID и PRD, что говорит о важности моделирования долгосрочных временных зависимостей в 10-секундных записях. Потеря VAE привела к умеренному ухудшению, что согласуется с его ролью как «морфологического энкодера» – в отличие от GNN, он не отвечает напрямую за биофизику.
Для оценки обобщающей способности модели использован независимый набор MIMIC-IV-ECG (n = 2 147 записей из отделений интенсивной терапии, длительность 10 с, частота дискретизации 500 Гц, SNR ≈ 15 дБ) [17]. По сравнению с валидационной выборкой PTB-XL наблюдается ожидаемая деградация метрик:
– FID = 0,068 ± 0,006;
– PRD = 16 ± 0,8 %;
– SE = 2,0 ± 0,2;
– доля сгенерированных сигналов с физиологически нормальным QT-интервалом (350–450 мс) составила 89,4 %, что на 3,7 % ниже показателя полной модели.
Ухудшение обусловлено смещением области (ICU-сигналы существенно более зашумленные, чем амбулаторные записи PTB-XL). Тем не менее полученные результаты подтверждают хорошую обобщаемость модели на разнородные клинические данные и ее готовность к применению в реальных условиях эксплуатации.
Несмотря на достигнутые результаты, у модели есть ряд ограничений. Во-первых, она не учитывает некоторые редкие патологии, которые встречаются в клинической практике. Во-вторых, генерация длительных записей (более 10 с) может приводить к накоплению артефактов из-за ошибок в процессе диффузии. В-третьих, текущая реализация требует значительных вычислительных ресурсов для генерации (GPU с 24 ГБ памяти).
Результаты, полученные в данной работе, имеют важное практическое значение для медицинских исследований. Синтетические данные, сгенерированные разработанной моделью, могут быть использованы:
– для обучения моделей диагностики редких аритмий;
– улучшения обобщающей способности существующих алгоритмов;
– снижения зависимости от дефицита аннотированных данных;
– обучения новых специалистов в кардиологии.
Заключение
В работе представлена гибридная модель VAE-GNN-SSSD для генерации физиологически корректных 12-канальных ЭКГ-сигналов длительностью 10 с. Предложенная архитектура успешно интегрирует вариационный автокодировщик для выделения морфологических компонент, графовую нейронную сеть с частично фиксированной матрицей смежности для соблюдения биофизических законов Эйнтховена и Вильсона и диффузионную модель со структурированным пространством состояний для моделирования долгосрочных временных зависимостей. На тестовой выборке PTB-XL модель достигла значений метрик FID = 0,052 и PRD = 10,8 %, продемонстрировав сопоставимое качество с передовыми аналогами при обеспечении уникального преимущества – встроенной биофизической корректности (MSE по закону Эйнтховена = 0,084).
Практическая значимость работы подтверждена успешным применением сгенерированных данных для аугментации обучающих выборок в задаче классификации аритмий на MIT-BIH. Аугментация позволила повысить Macro F1 на 6 % (с 0,84 до 0,89), значительно улучшить распознавание редких и клинически критичных классов (+5–7 % для желудочковых и фузированных сокращений) и снизить ложный пропуск опасных аритмий на 27 %. Модель также продемонстрировала высокую обобщающую способность на независимых ICU-данных (MIMIC-IV-ECG), что подтверждает ее готовность к применению в реальных клинических условиях для решения фундаментальной проблемы дефицита аннотированных данных при сохранении приватности пациентов.
1. World health statistics 2024. World Health Organization. Available at: https://www.who.int/data/gho/publications/world-health-statistics (accessed: 17.09.2025).
2. Shchetinin E. Yu. Sovremennye problemy cifrovoj obrabotki i analiza bol'shih dannyh v medicine i biologii: monografiya [Modern problems of digital processing and analysis of big data in medicine and biology: monograph]. Moscow, Izd. dom «Nauchnaya biblioteka», 2023. 168 p.
3. Shchetinin E. Yu., Pestryakova A. V. O modelirovanii elektrokardiogramm s korrelyaciej otvedenij metodami glubokogo obucheniya [On modeling electrocardiograms with lead correlation using deep learning methods]. Myagkie izmereniya i vychisleniya, 2025, no. 10, vol. 95, pp. 74-87. https://www.elibrary.ru/item.asp?id=83225498.
4. Naren Wulan, Wei Wang, Pengzhong Sun, Kuanquan Wang, Yong Xia, Henggui Zhang. Generating electrocardiogram signals by deep learning. Neurocomputing, 2020, vol. 404, pp. 122-136. https://doi.org/10.1016/j.neucom.2020.04.076.
5. Berger L., Haberbusch M., Moscato F. Generative adversarial networks in electrocardiogram synthesis: Recent developments and challenges. Artif. Intell. Med., 2023, vol. 143, p. 102632. DOIhttps://doi.org/10.1016/j.artmed.2023.102632.
6. Haradal S., Hayashi H., Uchida S. Biosignal Data Augmentation Based on Generative Adversarial Networks. Ann. Int. Conf. IEEE Eng. Med. Biol. Soc. 2018. Jul. Pp. 368-371. DOIhttps://doi.org/10.1109/EMBC.2018.8512396.
7. Kuznetsov V. V., Moskalenko V. A., Zolotykh N. Y. Electrocardiogram Generation and Feature Extraction Using a Variational Autoencoder. arXiv preprint arXiv, 2020, vol. 2002, p. 00240.
8. Berger L., Haberbusch M., Moscato F. Generative adversarial networks in electrocardiogram synthesis: Recent developments and challenges. Artificial Intelligence in Medicine, 2023, vol. 143, p. 102632. https://doi.org/10.1016/j.artmed.2023.102632.
9. Jiang Y. Research on Denoising Diffusion Probabilis tic Models. Highlights in Science, Engineering and Technology, 2024, vol. 107, pp. 560-572. doi.org/10.54097/sxd49274.
10. Hamilton W. L., Ying R., Leskovec J. Inductive Representation Learning on Large Graphs. Advances in Neural Information Processing Systems, 2017, vol. 30, pp. 1024-1034. DOIhttps://doi.org/10.48550/arXiv.1706.02216.
11. Gu A., Goel K., Ré C. Efficiently Modeling Long Sequences with Structured State Spaces. International Conference on Learning Representations (ICLR), 2022. Available at: https://openreview.net/pdf?id=uYLFoz1vlAC (accessed: 09.09.2025).
12. Zhao W., Bai L., Rao Y., Zhou J., Lu J. UniPC: A Unified Predictor-Corrector Framework for Fast Sampling of Diffusion Models. Advances in Neural Information Processing Systems, 2023. Available at: https://arxiv.org/abs/2302.04867 (accessed: 09.09.2025).
13. Wagner P., Strodthoff N., Bousseljot R. D., Kreiseler D., Lunze F. I., Samek W., Schaeffter T. PTB-XL, a large publicly available electrocardiography dataset. Sci Data., 2020, May 25, vol. 7 (1), p. 154. DOIhttps://doi.org/10.1038/s41597-020-0495-6.
14. Moody G. B., Mark R. G. The impact of the MIT-BIH Arrhythmia Database. IEEE Eng. Med. Biol. Mag., 2001, vol. 20 (3), pp. 45-50.
15. Neifar N., Ben-Hamadou A., Mdhaffar A., Jmaiel M. DiffECG: A Versatile Probabilistic Diffusion Model for ECG Signals Synthesis. 2024 IEEE/ACIS 22nd International Conference on Software Engineering Research, Management and Applications (SERA), 2024. Pp. 182-188. DOIhttps://doi.org/10.1109/SERA61261.2024.10685651.
16. Li X., Sakevych M., Atkinson G., Metsis V. Bio-Diffusion: A Versatile Diffusion Model for Biomedical Signal Synthesis. Bioengineering, 2024, vol. 11, p. 299. https://doi.org/10.3390/bioengineering11040299.
17. Johnson A. E. W., Bulgarelli L., Shen L., Gayles A., Shammout A., Horng S., Pollard T. J., Hao S., Moody B., Gow B., Lehman L.-W. H., Celi L. A., Mark R. G. MIMIC-IV, a freely accessible electronic health record dataset. Scientific Data, 2023, vol. 10, no. 1, art. 1. DOIhttps://doi.org/10.1038/s41597-022-01899-x.















