Россия
Два стада балтийской речной камбалы (Platichthys flesus trachurus) с различными особенностями жизненного цикла обитают в солоноватой воде Балтийского моря. Оба стада в летне-осенний период предпочитают прибрежные воды для нагула, но весной нерестятся в разных биотопах: в открытом море нерестится более крупная камбала, выметывающая пелагическую икру, в прибрежных районах – медленнорастущая более мелкая камбала, откладывающая донную икру. По результатам обловов в прибрежных водах в 2023 г. из 22 пойманных видов рыб балтийская речная камбала была доминирующей как по численности (39 %), так и по биомассе (55 %). Массовость вида четко прослеживалась на всех трех станциях исследования (ст. Светлогорск, Пионерский и Куликово). Максимальные уловы на усилие в поштучном (5,5 экз./сетесутки) и весовом (1,16 кг/сетесутки) выражениях приходились на ст. Пионерский. Кроме того, камбала оставалась самым многочисленным видом практически на всем периоде исследований с апреля по июль. Балтийская камбала является одним из компонентов «ядра» прибрежного ихтиоценоза Балтийского моря. Размерная структура камбалы строилась с применением кумуляты и рассматривалась в зависимости от таких факторов среды, как температура и глубина. На глубинах 0–5 м постоянно обитает стадо мелкоразмерной камбалы с прибрежным нерестом. По мере прогрева воды (до 10–19 °С и выше) в прибрежную зону после нереста начинает подниматься более крупная камбала на нагул. С увеличением глубины (5–10, 10–15 м) увеличивается и доля крупной камбалы. Это связано с изменением пропорций тела рыбы (с увеличением линейных размеров увеличивается и размер рта) и спектра ее питания: на мелководье в рационе преобладают ракообразные, тогда как на глубине – моллюски.
Балтийское море, камбала балтийская речная, видовая структура, размерная структура, температура, глубина
Введение
Балтийская речная камбала (Platichthys flesus trachurus) является в Балтийском море самой многочисленной и широко распространенной рыбой из семейства камбаловых. Донный вид бореального фаунистического комплекса. Эвригалинный: живет либо в соленой воде, либо в солоноватой и является единственной европейской камбалой, которая проникает высоко в эстуарии рек и способна жить в пресной воде в течение длительных периодов, обязательно возвращаясь весной в море для размножения. Камбала, которую ловят у берегов Калининградской области, принадлежит к Гданьскому и Борнхольмскому стадам, которые после пелагического нереста при солености более 11 ‰ идут на мелководье для нагула. Кроме того, существует стадо прибрежной медленно растущей камбалы, которая мечет демерсальную икру тут же у берегов (при солености менее 6 ‰). Нерестится над песчаным или каменистым грунтом на глубинах 5–50 м при температуре 2–3,5 ºС [1–4]. Таким образом, камбала образует локальные группировки, отличающиеся скоростью роста, временем полового созревания, сроками нереста, глубиной нахождения нерестилищ. Такие различия в жизненном цикле могут влиять на качественный и количественный состав прибрежного ихтиоценоза. Кроме того, любые временные изменения абиотических (температура, глубина, кислород, соленость) и биотических факторов (хищничество) могут влиять на размерную и пространственную структуры камбалы с течением времени. Эти знания могут быть важными для сохранения запасов с уникальными биологическими свойствами (определенная морфа или стадо, особенность жизненного цикла или локальная адаптация). В связи с этим целью работы было определение доли балтийской камбалы в видовой структуре прибрежного ихтиоценоза в весенне-летний период и анализ изменения размерной структуры вида в аспекте таких абиотических факторов, как температура и глубина.
Материал и методика
В работе использованы ихтиологические материалы комплексных рыбохозяйственных исследований сотрудников кафедры водных биоресурсов и аквакультуры ФГБОУ ВО «Калининградский государственный технический университет» за апрель–июль 2023 г. в прибрежной зоне Балтийского моря в пределах Калининградской области. Обловы проводились вдоль северного побережья Самбийского полуострова в районе станций Светлогорск, Пионерский и Куликово на глубинах от
0 до 20 м (рис. 1).
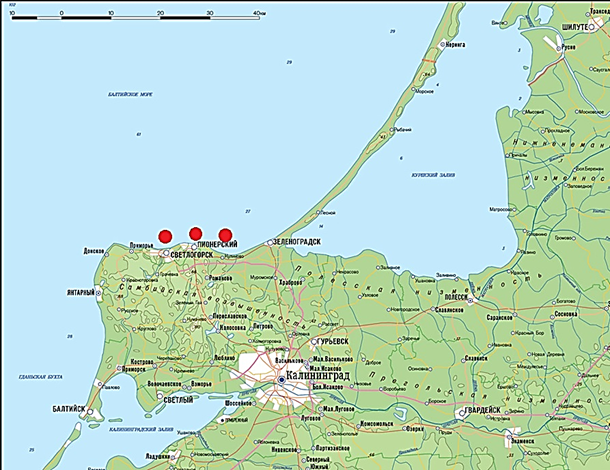
Рис. 1. Расположение станций проведения обловов в весенне-летний период 2023 г.
Fig. 1. Location of the fishing stations in the spring-summer period of 2023
Лов рыбы осуществлялся донными жаберными сетями с шагом ячеи 12, 14, 16, 18, 20, 22, 24, 30, 35, 40, 45, 50, 55, 60, 80 мм. Для глубин до 1,5 м использовалась мальковая волокуша длиной 10 м с шагом ячеи в кутке 5 мм. Всего было выполнено 507 обловов, в результате которых отловлено и подвергнуто анализу 9,5 тыс. экз. рыб различных видов. Стандартная обработка уловов включала массовые промеры с размерным интервалом 1 см. За стандартный показатель улова на усилие для сетных орудий лова принят улов на одну сеть длиной 25 м за сутки [5, 6]. Обработка данных велась в информационно-аналитической системе «Рыбвод». Размерная структура балтийской камбалы проанализирована с учетом таких абиотических факторов, как температура и глубина. Температура воды была поделена на диапазон низких температур – 0–9 ºС («нерестовые»), диапазон потепления – 10–19 ºС и температуры летних прогретых водных масс – выше 20 ºС. Во время исследований температура измерялась в поверхностном слое, затем ее значения распространялись на все глубинные слои, поскольку вертикальное распределение температуры характеризуется ее незначительным понижением до 20–30 м [7]. Глубины рассматривались в трех интервалах: 0–5, 5–10 и 10–15 м.
Размерная структура рыб обычно представляется гистограммой или вариационной кривой. В данном исследовании эта кривая имела «пилообразную» форму, что затруднило сопоставление нескольких таких кривых. В связи с этим для представления размерной структуры балтийской речной камбалы была использована кумулята. Оценка статистической значимости различий между размерными структурами проводилась с помощью критерия лямбда Колмогорова – Смирнова (λ0,95 = 1,36) [8].
Результаты и обсуждение
Видовая структура уловов. В Балтийском море обитает более 100 видов рыб [9, 10]. Ихтиофауна 26 подрайона Балтийского моря (районирование по классификации Международного совета по исследованию моря (ИКЕС)), примыкающего к административным границам Калининградской области Российской Федерации, представлена более чем 70 видами рыбообразных и рыб [1], из которых на глубинах от 0 до 20 м в результате наших многолетних исследований было обнаружено 32 вида рыб из 21 семейства [11]. За период настоящего исследования видовой состав уловов был представлен 22 видами из 15 семейств (табл.).
Видовой состав уловов в весенне-летний период 2023 г.
Species composition of catches in the spring-summer period of 2023
|
Семейство |
Название вида |
|
|
латинское |
русское |
|
|
Clupeidae (Сельдевые) |
Alosa fallax |
Финта |
|
Clupea harengus membras |
Сельдь балтийская (салака) |
|
Окончание таблицы
Ending of Table
|
Семейство |
Название вида |
|
|
латинское |
русское |
|
|
|
Sprattus sprattus balticus |
Шпрот балтийский (килька) |
|
Engraulididae (Анчоусовые) |
Engraulis encrasicholus |
Анчоус европейский |
|
Salmonidae (Лососевые) |
Salmo trutta trutta |
Кумжа (форель) |
|
Osmeridae (Корюшковые) |
Osmerus eperlanus |
Корюшка европейская |
|
Cyprinidae (Карповые) |
Carassius gibelio* |
Карась серебряный |
|
Rutilus rutilus |
Плотва |
|
|
Vimba vimba |
Рыбец |
|
|
Gadidae (Тресковые) |
Gadus morhua callarias |
Треска балтийская |
|
Syngnathidae (Игловые) |
Nerophis ophidion |
Игла северная змеевидная |
|
Syngnathus typhle |
Игла морская длиннорылая |
|
|
Percidae (Окуневые) |
Perca fluviatilis |
Окунь пресноводный |
|
Sander lucioperca** |
Судак |
|
|
Ammodytidae (Песчанковые) |
Ammodytes tobianus |
Песчанка балтийская |
|
Hyperoplus lanceolatus |
Песчанка большая |
|
|
Scombridae (Скумбриевые) |
Scomber scombrus |
Скумбрия атлантическая |
|
Gobiidae (Бычковые) |
Neogobius melanostomus |
Бычок-кругляк |
|
Cottidae (Рогатковые) |
Myoxocephalus scorpius |
Керчак европейский |
|
Cyclopteridae (Пинагоровые) |
Cyclopterus lumpus |
Пинагор |
|
Pleuronectidae (Камбаловые) |
Platichthys flesus trachurus |
Камбала речная балтийская |
|
Scophthalmidae (Калкановые) |
Scophthalmus maximus |
Тюрбо, большой ромб |
* В соответствии с Распоряжением Правительства РФ от 18 ноября 2017 г. № 2569-р: Carassius auratus gibelio; ** Stizostedion lucioperca.
Несмотря на разнообразие видового состава уловов, значительная доля пришлась на 5 видов: камбала балтийская, сельдь балтийская (салака), финта атлантическая, бычок-кругляк (по численности) и судак (по биомассе) (рис. 2, 3).
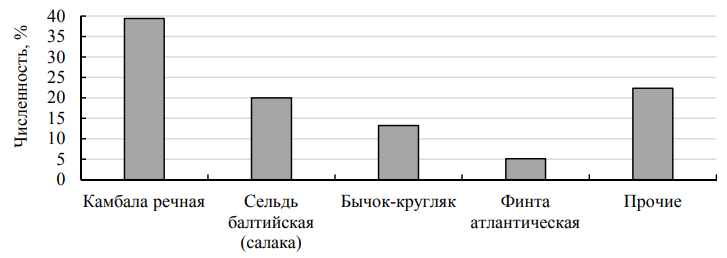
Рис. 2. Видовой состав уловов в весенне-летний период 2023 г. (по численности)
Fig. 2. Species composition of catches in the spring-summer period of 2023 (by number)
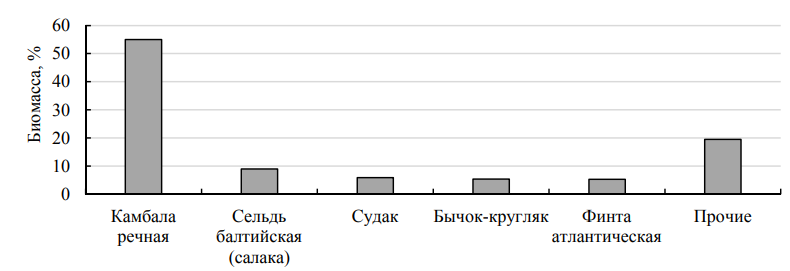
Рис. 3. Видовой состав уловов в весенне-летний период 2023 г. (по биомассе)
Fig. 3. Species composition of catches in the spring-summer period of 2023 (by number)
Балтийская камбала в контрольных уловах доминировала и по численности, и по биомассе – 39 и 55 % соответственно. На втором месте и по численности, и по биомассе была сельдь балтийская – 20 и 9 % соответственно. Третьим по численности был бычок-кругляк (13 %), тогда как по массе, при незначительной своей численности в 2 %, третьим становится судак (6 %), что объясняется его большей массой. В группу «прочие» входят виды, чья доля в уловах составила меньше 4 %: окунь пресноводный, камбала-тюрбо, треска, рыбец, плотва, кумжа, скумбрия атлантическая, песчанки балтийская и большая, корюшка европейская, карась серебряный, балтийская килька (шпрот), анчоус европейский, иглы змеевидная и длиннорылая, пинагор, керчак европейский и судак (в графике по численности). Из всех трех станций, на которых проводились контрольные обловы, только ст. Куликово демонстрирует безоговорочное доминирование камбалы балтийской (50,5 %) при практически равной незначительной численности других «массовых» видов рыб (от 7,7 до 14,2 %) (рис. 4), чему благоприятствуют обширные площади песчаных грунтов (на всех глубинах исследования).
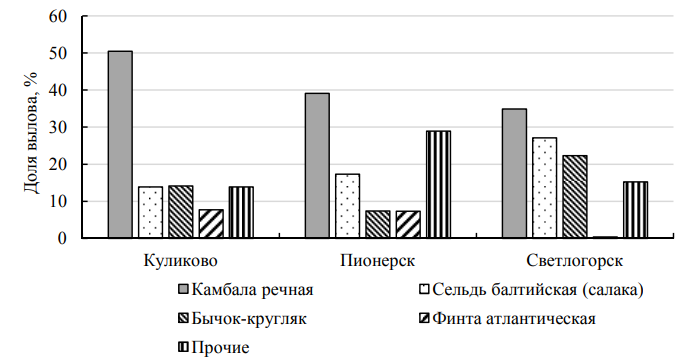
Рис. 4. Видовая структура уловов в 2023 г. по станциям
Fig. 4. Species structure of catches in 2023 by station
Станция Светлогорск отличается более разнообразными условиями жизни, в частности грунтами (разнофракционные пески, галька, валуны), что позволяет успешно сосуществовать пелагическим (сельдь) и донным видам (камбала на песке, бычок на камнях). Кроме того, в период исследований проходили строительные берегоукрепительные работы, которые повлекли образование зон высокой мутности воды, что способствовало привлечению балтийской сельди с образованием повышенных концентраций.
Максимальные уловы на усилие в поштучном (5,5 экз./сетесутки) и весовом (1,16 кг/сетесутки) выражении приходились на Пионерский, тогда как на других станциях эти показатели составили 2,9 экз./сетесутки и 0,57 кг/сетесутки на ст. Светлогорск, 2,2 экз./сетесутки и 0,39 кг/сетесутки на ст. Куликово.
На рис. 5 приведена видовая структура контрольных обловов для массовых видов по месяцам.
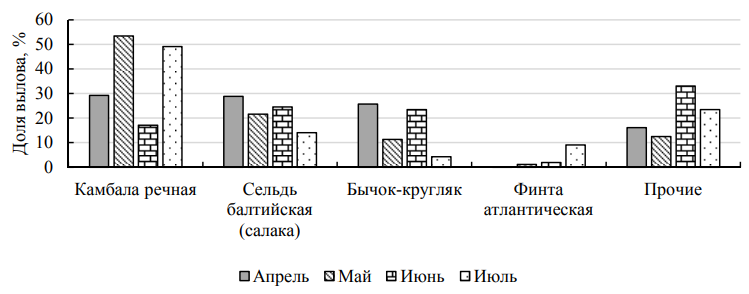
Рис. 5. Видовая структура уловов в 2023 г. по месяцам
Fig. 5. Species structure of catches in 2023 by month
На гистограмме прослеживаются два пика (53 и 49 %) доминирования балтийской камбалы: в мае происходит массовый нерест мелкой расы на отмелях вблизи берегов, а в июле наблюдается присутствие другой, более крупной расы, которая поднимается с глубины после нереста на нагул. В июне доля камбалы (17 %) уступает другим видам рыб (с более поздними сроками размножения), которые в этот период могут подходить к берегу и образовывать нерестовые скопления. Размерная структура камбалы. Размерная структура балтийской речной камбалы на глубинах до 5 м при самых низких температурах была представлена 23 размерными классами – от 10 до 33 см с преобладанием групп от 19 до 25 см (57,2 %) (рис. 6).
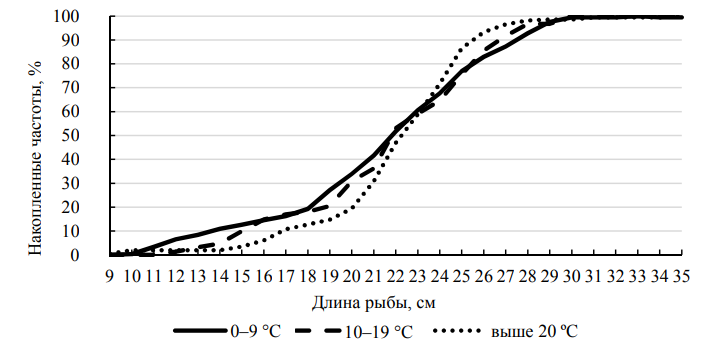
Рис. 6. Размерная структура балтийской камбалы в зависимости от температуры на глубинах 0–5 м
Fig. 6. The size structure of the Baltic flounder depending on the water temperature at depths of 0-5 m
При температурах воды среднего диапазона фиксировалась рыба 19 размерных классов (от 12 до 30 см), а 7 основных классов (от 20 до 26 см) пришлось 65,1 %. И, наконец, при температуре выше 20 ºС размерная структура включала 23 класса – от 9 до 31 см со значительным преобладанием рыб лишь 5 классов – от 21 до 25 см, что составило 67,1 %. Для всех трех температурных диапазонов модальная группа составила 22 см. Размерные структуры балтийской камбалы в диапазоне глубин 0–5 м достоверно различаются при температурах 0–9 и выше 20 ºС при уровне значимости α = 0,05 (λ = 1,45). С повышением температуры воды наблюдается миграция большего количества крупной рыбы на мелководье. Подобная картина возможна летом, когда в теплые, богатые кормовыми ресурсами воды с глубины поднимается крупная раса камбалы.
На глубинах от 5 до 10 м больше всего классов наблюдалось в размерной структуре камбалы при температуре воды выше 20 ºС – 23 класса (от 9 до 32 см), из которых основную массу (47,1 %) составили рыбы четырех классов – от 20 до 23 см. Модальная группа – 22 см (рис. 7).
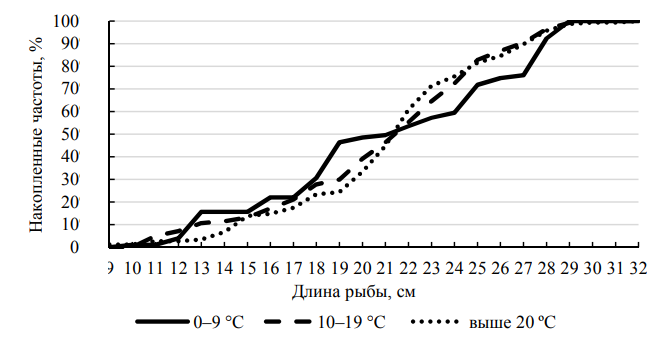
Рис. 7. Размерная структура балтийской камбалы в зависимости от температуры на глубинах 5–10 м
Fig. 7. The size structure of the Baltic flounder depending on the water temperature at depths of 5-10 m
Размерные структуры двух других температурных диапазонов состояли из 19 размерных классов: 10–29 см при низких температурах (мода – 28 см)
и 11–30 см (мода – 25 см) при температурах среднего диапазона (численное преобладание было за размерными группами 20–25 см, что составило 52,8 %). При низких температурах воды камбала в уловах была малочисленна, возможно, рыба находилась здесь временно, предпочитая мелководье, и ее поимка носит скорее случайный характер.
Размерная структура камбалы при температуре 0–9 ºС достоверно различается с размерными структурами при температурах 10–19 и выше 20 ºС, критерий λ составил 1,64 и 2,21 соответственно (α = 0,05). Размерная структура балтийской камбалы на глубинах от 10 до 15 м при температурах до 9 ºС была представлена классами от 11 до 29 см (преобладающими размерами стали 20–24 см, что составило 50,6 %), в диапазоне 10–19 ºС – от 10 до 29 см (55,9 % приходится на размерные классы 21–24 см). Модальная группа для описанных диапазонов – 22 см (рис. 8).
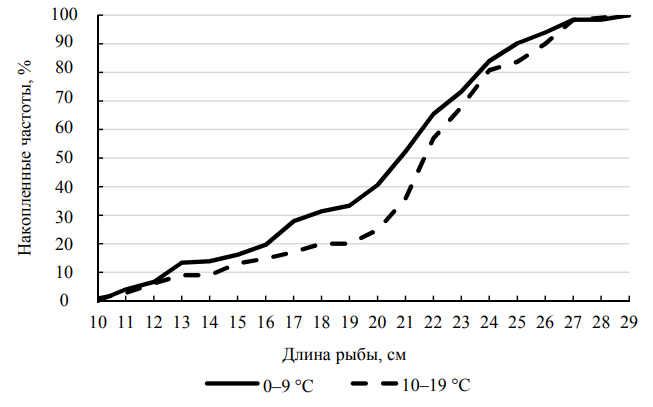
Рис. 8. Размерная структура балтийской камбалы в зависимости от температурына глубинах 10–15 м
Fig. 8. The size structure of the Baltic flounder depending on the water temperature at depths of 10-15 m
При температуре выше 10 ºС преобладают более крупные особи (см. рис. 8). В летний период вместе с прогревом воды начинается откорм поднимающейся с глубины быстрорастущей расы. Такая рыба предпочитает в питании более крупных моллюсков, которые держатся дальше от берега на большей глубине. Так, по литературным данным [12], пища камбал, обитающих на глубине 1 м, в основном состоит из ракообразных, на глубине 15 м – из моллюсков. Представленные размерные структуры балтийской камбалы достоверно различаются при уровне значимости α = 0,05, критерий λ составил 1,64.
Заключение
По результатам обловов в 2023 г. из 22 пойманных видов рыб балтийская речная камбала была доминирующим видом как по численности, так и по биомассе. Кроме того, камбала была самым массовым видом в видовых структурах уловов по станциям исследования (ст. Светлогорск, Пионерский и Куликово) и по месяцам обловов (кроме июня). Таким образом, можно сделать вывод, что камбала является одним из компонентов «ядра» прибрежного ихтиоценоза Балтийского моря. Размерная структура камбалы, по результатам исследований в весенне-летний период 2023 г., была представлена особями от 9 до 33 см. В прибрежной зоне на глубинах до 5 м постоянно обитает мелкая камбала. По мере прогрева воды (до 10–19 °С и выше) после нереста на нагул с глубины начинает подниматься более крупная камбала. На глубинах 5–10 и 10–15 м доля крупной камбалы увеличивается, что связано с изменением спектра ее питания: на мелководье в рационе преобладают ракообразные, тогда как на глубине – моллюски. Наблюдение за размерной структурой камбалы во времени позволит отследить и проанализировать реакцию вида на новые условия обитания. Запасы рыб могут по-разному реагировать на изменения окружающей среды (затоки соленой североморской воды, уровни концентрации кислорода и пр.) и давление рыболовства. Эти факты особенно значимы в эпоху быстрого изменения климата, прибрежной эвтрофикации и перелова. Так, повышение средней температуры морской воды повлечет сокращение районов обитания и нерестилищ камбалы, ухудшение условий нагула и роста взрослых особей, снижение выживаемости икры и молоди. Кроме того, более высокие температуры ускоряют процессы окисления органических веществ, приводящие к уменьшению содержания кислорода в воде. Все более расширяющиеся зоны гипоксии создают стрессовые условия для морских организмов.
Происходящие в Балтийском море изменения могут привести к трансформации трофических цепей, коррекции условий и сроков нереста массовых видов рыб, в том числе и балтийской речной камбалы. Пространственно-временное отслеживание вкла-да различных генетических популяций (рас, морф) в смешанный промысел может сыграть ключевую роль в будущем адаптивном управлении, направленном на предотвращение ухудшения рыболовства. Такое управление может оказаться лишь частично зависимым от местного прессинга рыболовства и быть связано с изменениями окружающей среды, происходящими на нерестилищах на значительном расстоянии от мест ведения промысла.
1. Тылик К. В. Ихтиофауна Калининградской области: справ. пособие. Калининград: Изд-во КГТУ, 2003. 128 с.
2. Бетешева Е. И., Куликова Е. Б. Речная камбала (Pleuronectes flesus trachurus, Duncker) средней части Балтийского моря // Тр. ВНИРО. 1953. T. XXVI. C. 102–117.
3. Nissling A., Westin L., Hjerne O. Reproductive suc-cess in relation to salinity for three flatfish species, dab (Limanda limanda), plaice (Pleuronectes platessa), and flounder (Pleuronectes flesus), in the brackish water Baltic Sea // ICES Journal of Marine Science. 2002. V. 59 (1). Р. 93–108.
4. Фукс Г. В. Биология речной камбалы Platichthys flesus (Linnaeus, 1758) реки Пеша // Природные ресурсы, их современное состояние, охрана, промысловое и техническое использование: Нац. (всерос.) науч.-практ. конф. Петропавловск-Камчатский: КамчатГТУ, 2024. С. 144–148.
5. Правдин И. Ф. Руководство по изучению рыб. М.: Пищ. пром-сть, 1966. 376 с.
6. Шибаев С. В., Соколов А. В. Метод анализа ихтиоценозов малых озер Калининградской области на основе контрольных обловов сетных орудий лова // Тр. ВНИРО. 2014. Т. 151. С. 158–164.
7. Балтийское море. Гидрохимия // Единая государственная система информации об обстановке в Мировом океане (ЕСИМО). URL: http://esimo.oceanography.ru/esp2/index/index/esp_id/1/section_id/7/menu_id/4583 (дата обращения: 18.05.2025).
8. Плохинский Н. А. Биометрия. М.: Изд-во МГУ, 1970. 186 с.
9. Environment of the Baltic Sea Area 1994-1998 // Baltic Sea Environ-ment Proceedings № 82B. HELCOM, 2002. 216 p.
10. Гущин А. В., Федоров В. Е. Современное состояние промысловой ихтиофауны южной части Балтийского моря как следствие антропогенного воздействия // Уч. зап. Рос. гос. гидрометеоролог. ун-та. Науч.-теорет. журн. 2017. Т. 49. С. 134–144.
11. Шибаев С. В., Новожилов О. А., Алдушин А. В., Бурбах А. С., Алдушина Ю. К., Гулина Т. С., Барановский П. Н., Федоров Л. С. Исследование видового состава прибрежного ихтиоценоза Балтийского моря в Калининградской области // Вопр. рыболовства. 2024. Т. 25 (1). С. 49–58.
12. Бетешева Е. И., Желтенкова М. В. Биология и промысел речной камбалы средней части Балтийского моря. М.: Пищепромиздат, 1951. 24 с.
















