Russian Federation
Russian Federation
Russian Federation
Polysaccharides are the most widely used biopolymers in the food industry, for example sodium alginate (food additive E401) taken as an anionic substance. Sodium alginate can act as a thickening agent in jelly-like materials, fillings and gravy products, and as a moisture-retaining ingredient in baked goods and other products. The unique industrial source of sodium alginate in modern conditions is sea brown algae (kelp and fucus). In the Caspian basin Ectocarpus algae can be attributed to the brown algae species rich in alginates. Dry Ectocarpus served as the object of scientific analysis. At present, the emergence of new information on the pharmacological parameters of a number of algae biocomponents has led to an increased interest in the study of technological approaches to the production of functional food substances and their biologically active substances. At the same time, algae can act as a raw material base for producing both independent materials and their derivatives in the form of food premixes leading to an increase in the quality indicators of basic materials while maintaining taste sensations or improving the structural organization, external state and increasing storage time. The purpose of this study was to identify the static patterns of the ratio of the extractant masses and the object of study and the kinetics of extraction of the target components from the dry Ectocarpus with a aqueous-alcohol composition to determine the efficiency and rational time of this operation. The type of kinetic dependences of extraction does not contradict the approved and published data in this field with certain specifics for the product under study and the conditions for this operation. This determines the rationality of the original approaches to improve the efficiency of algal raw materials extraction in the above-mentioned extractant environment.
brown algae, Ectocarpus, sodium alginate, extraction, kinetics, extractant
Введение
Наиболее широко востребованными в пищевой индустрии биополимерами служат полисахариды, например натриевый альгинат (пищевая добавка Е401) как анионная субстанция. Данное вещество является гелеформирующим премиксом водных растворов при смешении с натриевыми солями и/или отрицательно заряженных полимерных комплексов [1]. Альгинат натрия хорошо зарекомендовал себя в качестве загустителя при производстве изделий в желе, соусах и заливках, используется как влагоудерживающий ингредиент в хлебе и хлебобулочных изделиях и др. [2–4]. Принимая во внимание исследование [5], можно сделать заключение о том, что бурые водоросли морской природы (ламинария и фукус) в современных условиях служат уникальным индустриальным источником альгината натрия. В отдельных государствах выработка альгината натрия проводится по специфическим технологическим путям, но в основе своей принципы извлечения альгината натрия из водорослевого сырья (ВС) подобны [6].
В Каспийском бассейне преобладающими являются диатомовое (292 типа) и зеленое (139 типов), ВС присутствующие преимущественно в пресной водной среде, а также – реже – в солоноватых и морских водных ареалах, и сине-зеленое (203 типа) [7]. Иные подвиды ВС встречаются реже, так, например, присутствует 13 типов бурого ВС, к которому можно причислить эктокарпус [8], а учитывая, что к числу видов, богатых на альгинат натрия, относятся бурые водоросли, этот вид нитевидных водорослей семейства эктокарпусовых представляет особый интерес.
Эктокарпус – макроскопическая (до 60 см) водоросль, нитчатая гетеротрихальная, имеющая вид ветвистых. Альгинаты образуют основной структурный полисахарид многих морских бурых водорослей, и эктокарпус не является исключением [9].
На настоящий момент, при владении информа-
цией о фармакологических параметрах ряда биокомпонентов ВС, в мировой практике появился повышенный интерес к разработке технологических подходов к производству пищевых субстанций функционального назначения из ВС и их биологически активных веществ. При этом ВС может служить сырьевой базой для выработки как самостоятельных материалов, так и их производных в качестве пищевых премиксов, приводящих к росту качественных показателей базовых материалов при сохранности вкусовых ощущений или улучшении структурной организации, внешнего состояния и росте продолжительности хранения [10]. Все это говорит в пользу перспективности создания технологии комплексной переработки ВС, не затрагивая ее основные этапы по получению альгината натрия, а значит, требуется научно обоснованная корректировка подготовительных операций, целью которой ставится максимально возможное извлечение ценных веществ из бурых водорослей, в частности эктокарпуса.
По рекомендуемой технологии сырое ВС очищается от нежелательных включений и поступает на диспергирование и обезвоживание и далее на экстрагирование 65–75 %-м раствором этанола при объемных долях ВС и экстрагента 1 : (5–10), температуре 50–60 °С, длительности операции 1,5–2,5 ч и периодическом перемешивании. По завершении операции проводят разделение посредством фильтрации рафината ВС, который поступает на выработку полисахаридов, и экстракта, подаваемого на отгонку спиртовой среды. Далее из очищенного экстракта вырабатывают водожировую композицию, снижая ее температуру до 5–10 °С и осаждая ее для отделения воды от жиров.
Выявить статические закономерности, соотношение масс экстрагента и объекта изучения и кинетику экстракции целевых компонентов из сухого эктокарпуса водно-спиртовой композицией необходимо для определения эффективности и рационального времени течения данной операции.
Объекты и методы исследования
Объектом исследования послужил эктокарпус в сухом и измельченном виде.
Эксперимент проводился в несколько этапов.
1. Определяется насыпная плотность ВС, высушенного до конечной влажности 18 % ρн, кг/м3, т. к. данный показатель необходим для получения корректного объемного соотношения «сырье : экстрагент».
2. При максимуме допустимых долей ВС и экстрагента 1 к 10 из диспергированного сухого ВС экстрагируют 70 %-м водным раствором этанола при 60 °С 2,5–3,0 ч в экстракторе Сокслета, который был модернизирован специально для этой цели, с учетом отсутствия необходимости для экстрагента менять свое агрегатное состояние. Далее рафинат ВС отводили от экстракта посредством фильтрации.
3. Из экстракта отгоняют при пониженном давлении растворитель посредством роторной испарительной установки до снижения его первоначального объема в 3 раза, после чего концентрированный экстракт подвергается дальнейшему концентрированию в сушильном шкафу до максимально возможного удаления растворителя из экстракта, до получения обезвоженного экстракта, и по его весу находят выход целевых компонентов из ВС.
4. Находят рациональные массовые доли экстрагента и диспергированного высушенного ВС и проводят экстракцию из него 70 %-м водным раствором этанола при 60 °С в течение 2,5–3,0 ч при варьируемых долях экстрагента и ВС.
Экспериментальное определение ρн заключается во взвешивании сухого сырья в заданном объеме мерного цилиндра, которое оно занимает при его засыпании в емкость только при наличии силы тяжести.
Экспериментальное определение итоговой концентрации сухих веществ в полученном экстракте для выявления ее текущего значения в процессе экстрагирования осуществлялось на опытном стенде (рис. 1).
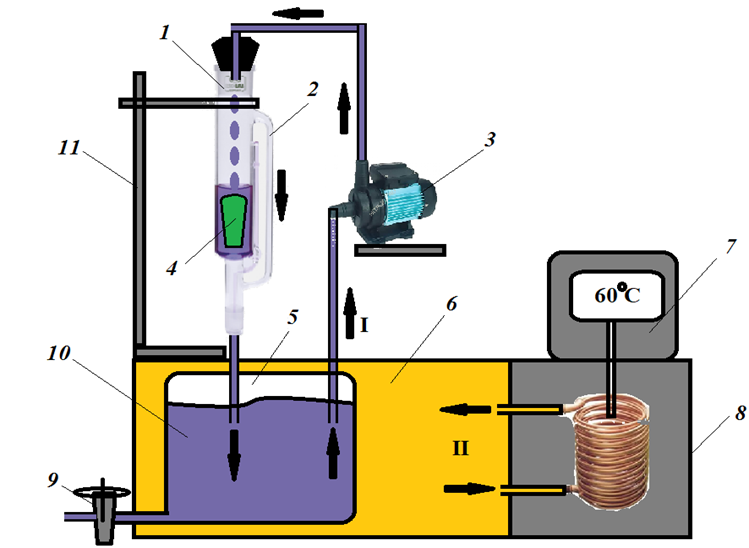
Рис. 1. Схема опытного стенда: I – поток экстрагента; II – поток теплового агента;
1 – экстрактор Сокслета; 2 – сифон экстрактора; 3 – насос; 4 – сырье; 5 – емкость для сбора экстракта;
6 –тепловой агент; 7 – блок управления термостатом; 8 – термостат; 9 – сливной кран;
10 – получаемый экстракт; 11 – штатив
Fig. 1. Scheme of the experimental stand: I – extractant flow; II – heat agent flow;
1 – Soxhlet extractor; 2 – extractor siphon; 3 – pump; 4 – raw materials; 5 – container for collecting the extract;
6 – thermal agent; 7 – thermostat control unit; 8 – thermostat; 9 – drain valve; 10 – extract obtained; 11 – holder
Представленная на рис. 1 лабораторная экстракционная установка позволяет проводить изучаемый массообменный процесс при различных температурах растворителя, что невозможно при использовании напрямую экстрактора Сокслета, при этом все остальные достоинства этого аппарата сохраняются. Центральная трубка соединяется с боковой (сифоном) как сообщающаяся емкость, которая одним концом вводится в резервуар с получаемым экстрактом, и появляющаяся над гильзой выше сифонной трубки жидкая среда с растворенной субстанцией стекает книзу. Таким образом, процесс избирательного извлечения целевых веществ из растительного сырья можно повторять многократно, добиваясь максимального их экстрагирования при варьируемых температурных режимных параметрах экстрагента.
Экспериментальное определение рационального объемного соотношения экстрагента и объекта экстрагирования осуществлялось на том же стенде в течение 180 мин, что, согласно постановочным экспериментам, является достаточным для установления равновесия между экстрагентом и ВС.
Выявление кинетических закономерностей экстрагирования осуществлялось при трех различных условиях:
1. Настаивание:
– температура экстрагента – 60 °С;
– объемное соотношение «сырье : экстрагент» – V ≈ 1 : 8;
– начальная влажность ВС – W ≈ 18 %;
– встряхивание суспензии – 1 раз в 10 мин.
2. Экстракция с механическим перемешиванием суспензии:
– температура экстрагента – 60 °С;
– объемное соотношение «сырье : экстрагент» – V ≈ 1 : 8;
– начальная влажность ВС – W ≈ 18 %;
– скорость перемешивающего устройства (окружная скорость конца лопастей) – v ≈ 1 м/с.
3. Циркуляционное экстрагирование на установке (см. рис. 1):
– температура экстрагента – 60 °С;
– объемное соотношение «сырье : экстрагент» – V ≈ 1 : 8;
– начальная влажность ВС – W ≈ 18 %;
– продолжительность цикла – τц ≈ 4 мин.
Результаты и их обсуждение
Результаты проведенного исследования по определению насыпной плотности объекта представлены в табл. 1
Таблица 1
Table 1
Данные экспериментов по определению насыпной плотности объекта исследования
Experimental data on determining the bulk density of the object of study
|
Номер |
Масса образца |
Занимаемый объем, мл |
Насыпная плотность образца, кг/м3 |
|
1 |
6,8 |
100 |
68 |
|
2 |
6,5 |
65 |
|
|
3 |
7,0 |
70 |
|
|
4 |
6,3 |
63 |
|
|
5 |
6,4 |
64 |
|
|
Среднее значение |
66 |
||
Результаты проведенных исследований по определению итоговой концентрации сухих веществ в полученном экстракте при максимальном объемном соотношении «сырье : экстрагент» (1 : 10) представлены в табл. 2.
Таблица 2
Table 2
Данные экспериментов по определению концентрации сухих веществ в экстракте
Experimental data on determining the concentration of solids in the extract
|
Номер |
Масса отобранного |
Масса сухого остатка, г |
Итоговая концентрация целевых веществ в экстракте, % |
|
1 |
1,802 |
0,002 |
0,111 |
|
2 |
4,545 |
0,004 |
0,088 |
|
3 |
2,084 |
0,002 |
0,096 |
|
4 |
2,970 |
0,003 |
0,101 |
|
5 |
3,389 |
0,002 |
0,059 |
|
Среднее значение |
0,091 |
||
В табл. 3 сведены данные эмпирического изучения, причем рациональные массовые доли экстрагента и ВС были определены расчетным путем, учитывая уже известные на текущий момент плотностные характеристики как ВС (ρ = 905 кг/м3 и ρн = 66 кг/м3), так и экстрагента (ρэ = 868 кг/м3) [11].
Таблица 3
Table 3
Данные для определения рациональных долей растворителя и водорослевого сырья
Data on determining the rational proportions of the solvent and algal raw materials
|
Вариант |
Объем сырья / |
Масса отобранного экстракта, г |
Масса сухих веществ, г |
Концентрация |
Удельный выход, % |
|
1 |
150/75 |
4,03 |
0,005 |
0,125 |
8,2 |
|
2 |
125/75 |
2,54 |
0,003 |
0,119 |
9,3 |
|
3 |
110/75 |
3,45 |
0,004 |
0,117 |
10,5 |
|
4 |
95/75 |
2,63 |
0,003 |
0,114 |
11,9 |
|
5 |
85/75 |
3,16 |
0,003 |
0,096 |
11,1 |
|
6 |
75/75 |
2,2 |
0,002 |
0,092 |
11,9 |
Полученные данные свидетельствуют о том, что четвертый вариант наиболее рационален для осуществления операции экстракции ВС, согласно чему 6,27 г подготовленного ВС (0,066 г/мл ∙ 95 мл = 6,27 г) при его влажности W = 18 % соответствует 651 г 70 %-го раствора этанола (0,868 г/мл ∙ 750 мл = 651 г). Итак, считаем, что рациональным вариантом являются массовые доли ВС и экстрагента 1 к 100, а объемные – 1 к 8.
Анализ опытных данных по экстрагированию из ВС при определенных условиях осуществления процесса показал, что максимальное время данной процедуры составило 4 ч, а минимальное – 2 ч. В результате получены кривые экстракции целевых веществ (рис. 2) из предварительно обезвоженного и измельченного эктокарпуса.
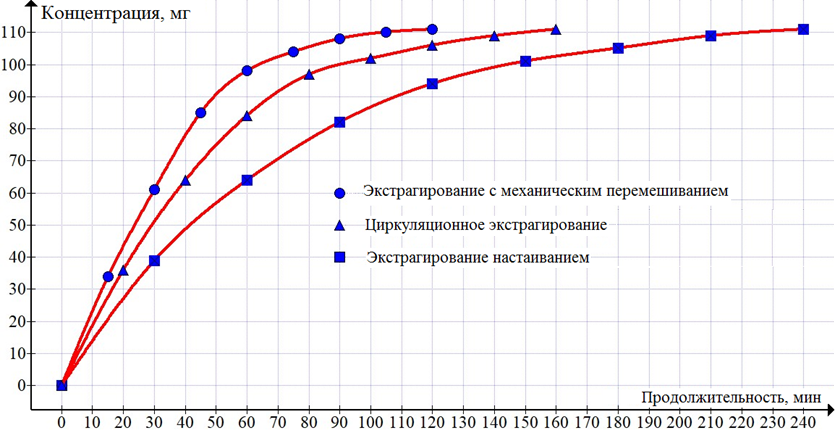
Рис. 2. Кривые экстрагирования
Fig. 2. Extraction curves
Проведена математическая аппроксимация опытных кривых (см. рис. 2) с целью получения кинетических зависимостей, причем для упрощения их математической обработки и получения целевой функции ![]() выявлены обратные зависимости
выявлены обратные зависимости ![]() , которые представлены на рис. 3.
, которые представлены на рис. 3.
Кривые экстрагирования, представленные на рис. 3, были аппроксимированы полиномом третьей степени (рис. 4).
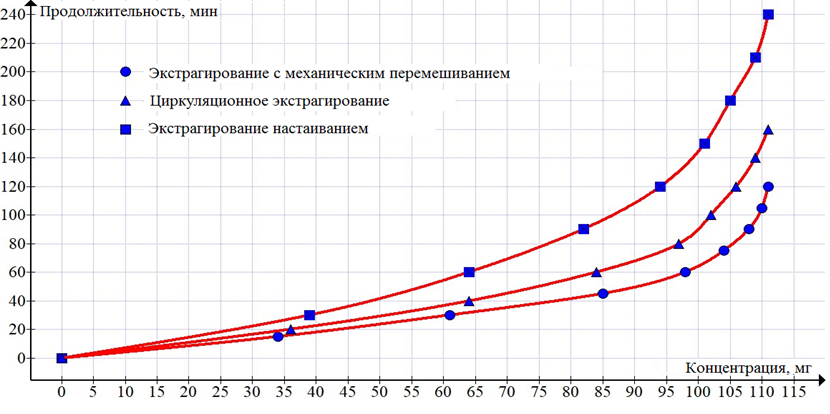
Рис. 3. Кривые экстрагирования (обратная зависимость)
Fig. 3. Extractionc curves (reverse dependence)
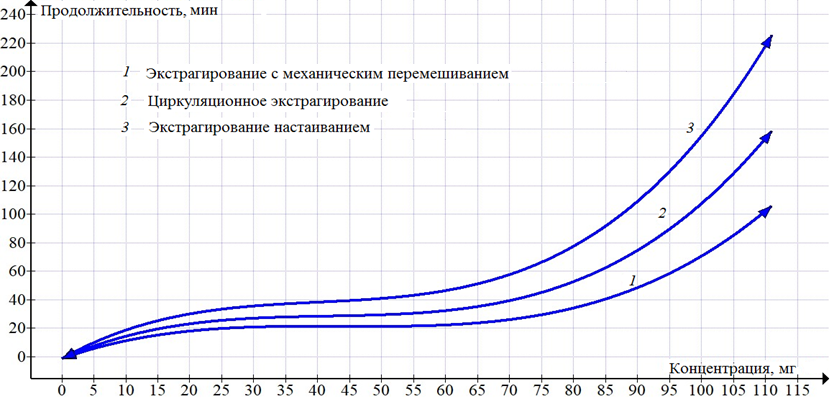
Рис. 4. Кривые экстрагирования (аппроксимированные зависимости)
Fig. 4. Extraction curves (approximate dependencies)
Ниже представлены полученные математические зависимости:
– настаивание:
![]()
– экстракция с механическим перемешиванием суспензии:
![]()
– циркуляционное экстрагирование на установке:
![]()
где Cx – концентрация сухих веществ в экстракте, мг/100 г; τ – время, мин.
После взятия производной от τ = f(Cx) имеем ![]()
![]() и далее
и далее ![]() .
.
– настаивание:
![]()
– экстракция с механическим перемешиванием суспензии:
![]()
– циркуляционное экстрагирование на установке:
![]()
На рис. 5 представлены полученные математические зависимости, описывающие скорость экстракции водо-спирторастворимых компонентов из ВС, в графической интерпретации.
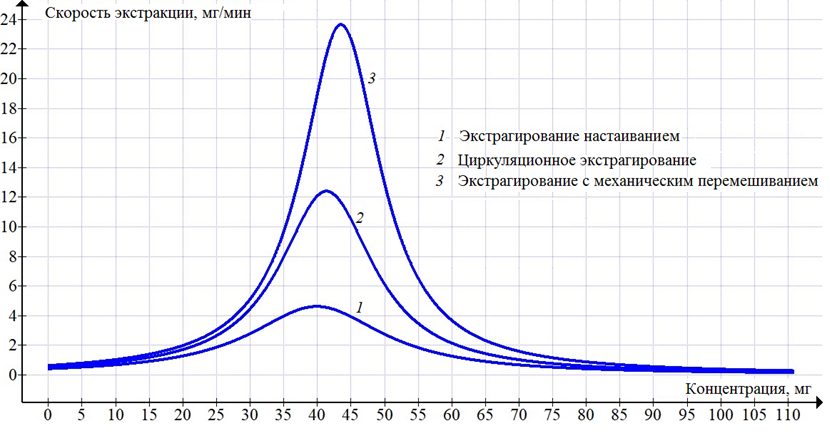
Рис. 5. Кинетические кривые экстрагирования
Fig. 5. Kinetic extraction curves
Изучение опытных данных свидетельствует о том, что на кинетической кривой присутствуют две стадии течения операции, что согласуется с теорией и известными результатами исследования экстракции [12–14]. На 1-й стадии экстрагирования повышение скорости экстракции можно объяснить применением дополнительного воздействия, например мешалкой, которое обусловливает нарушение структуры частиц водоросли, что способствует интенсификации высвобождения и переноса целевых компонентов из них, а также повышением температуры объекта за счет взаимодействия с горячим экстрагентом, что, кроме всего прочего, обусловливает увеличение интенсивности переноса компонентов посредством, в том числе, термо- и бародиффузии. Впоследствии по причине падения движущей силы массопереноса при уменьшении концентрации целевых веществ в рафинате и повышения в экстрагенте можно объяснить падение скорости экстракции на 2-й стадии.
Заключение
В итоге проведенного исследования выявлены статические закономерности, соотношение масс экстрагента и объекта изучения и кинетика экстракции целевых компонентов из сухого эктокарпуса водно-спиртовой композицией для определения эффективности и рационального времени течения данной операции.
Следует отметить, что вид кинетических зависимостей экстракции не противоречит известным апробированным и опубликованным данным в этой области при определенной специфике для изучаемого продукта и условий проведения этой операции. Это обусловливает резонность оригинальных подходов для повышения эффективности экстрагирования водорослевого сырья в вышеобозначенной среде экстрагента.
1. Vereschagin A. L., Kukarina E. A., Greshnyh E. V. Geleobrazovanie v sisteme kaolin - al'ginat natriya - sul'fat kal'ciya - pirofosfat natriya // Yuzhno-Sibir. nauch. vestn. 2021. № 6 (40). S. 3-9.
2. Cherkasov A. A., Chernyshev A. A., Lytkina D. N., Kurzina I. A. Poluchenie i issledovanie svoystv gidrogeley sostava: polivinilovyy spirt - al'ginat natriya // Vestn. Tom. gos. un-ta. Himiya. 2020. № 19. S. 6-13.
3. Ishevskiy A. L., Uspenskaya M. V., Gun'kova P. I., Davydov I. A., Vasilevskaya I. A. Napravleniya ispol'zovaniya al'ginatov v pischevoy promyshlennosti // Izv. Sankt-Peterb. gos. tehnolog. in-ta (Tehnich. un-ta). 2019. № 51 (77). S. 61-69.
4. Giro T. M., Andreeva S. V., Kulikovskiy A. V., Giro A. V. Vliyanie biorazlagaemogo plenochnogo pokrytiya na sohrannost' essencial'nyh veschestv // Vse o myase. 2022. № 1. S. 53-57.
5. Zaporozhec E. Yu., Nugmanov A. H.-H. Perspektivy polucheniya al'ginata natriya iz buryh vodorosley Kaspiyskogo morya // Vestn. Astrahan. gos. tehn. un-ta. 2022. № 2 (74). S. 48-53.
6. Podkorytova A. V., Shmel'kova L. P. Poluchenie al'ginata natriya iz othodov pri obrabotke laminarievyh // Izv. TINRO. 1983. T. 108. S. 53-56.
7. Novichenko O. V., Ryabuhin Yu. I., Magzanova D. K. Izuchenie effektivnosti adsorbiruyuschey sposobnosti vysshimi vodnymi rasteniyami del'ty reki Volgi i Severnogo Kaspiya nekotoryh tyazhelyh elementov-metallov // Tehnologii pischevoy i pererabatyvayuschey promyshlennosti APK - produkty zdorovogo pitaniya. 2021. № 3. S. 141-146.
8. Zinova A. D. Opredelitel' zelenyh, buryh i krasnyh vodorosley yuzhnyh morey SSSR. M.; L.: Nauka, 1967. 398 s.
9. Bixler H. J., Porse H. A decade of change in the sea-weed hydrocolloids industry // Journal of Applied Phycology. 2012. V. 23. P. 321-335.
10. Kotelnikova L. Kh., Podkorytova A. V., Roshchina A. N., Shashkina I. A. Beverages and desserts with therapeutic and prophylactic properties based on alginate-containing biogel from laminaria - “Vitalgar Cardio”. Dubai, UAE: KNE LIFE SCIENCES, 2022. P. 251-258.
11. Rabinovich V. A., Havin Z. Ya. Kratkiy himicheskiy spravochnik. L.: Himiya, 1978. S. 280.
12. Grishin N. S., Ponikarov I. I., Ponikarov S. I., Grishin D. N. Ekstrakciya v pole peremennyh sil. Gidrodinamika, massoperedacha, apparaty: monogr.: v 2 ch. Kazan': Izd-vo KNITU, 2012. Ch. 1. 468 s.
13. Grishin N. S., Ponikarov I. I., Ponikarov S. I., Grishin D. N. Ekstrakciya v pole peremennyh sil. Gidrodinamika, massoperedacha, apparaty: monogr.: v 2 ch. Kazan': Izd-vo KNITU, 2016. Ch. 2. 444 s.
14. Treybal R. E. Zhidkostnaya ekstrakciya: per. s angl. / pod red. d-ra tehn. nauk S. Z. Kagana. M.: Himiya, 1966. 724 s.
















