Russian Federation
Russian Federation
Esters occupy a special place in the field of chemistry of oxygen-containing acetylene derivatives due to the presence of highly reactive centers. Acetylene esters of glycols under acid-catalytic hydration conditions usually form ketoxyesters. The article set the task of finding ways to synthesize previously unknown mono- and dipropargyl esters of glycols, as well as to study their synthetic potential and practical use. The results of a study of acid-catalytic intramolecular cyclohydration and synthesis of heterocyclic compounds based on propargyl esters of glycols are presented. The latter were monopropargyl esters of 2,3- and 1,3-butanediols (I, II), which were obtained by condensation of propargyl alcohol with the corresponding glycols. Monopropargyl esters of 2,3-butanediol (I) was subjected to unusual transformations under the conditions of the hydration reaction. It was found that the monopropargyl ether of 2,3-butanediol (I), when heated in a vacuum with KOH, turns not into an individual product, but into a mixture of 4,5-dimethyl-2-vinyl-1,3-dioxolan (IV) and 3,5,6-trimethyl-1,4-dioxene (V). In an individual form, vinyl substituted 1,3-dioxane (VI) was obtained by counter synthesis by condensation of 1,3-butanediol with acrolene. Using the propensity of propargyl compounds to change in the basic medium, the possibility of converting monopropargyl esters of 2,3- and 1,3-butanediols (I, II) into oxygen-containing heterocycles was studied. The structure of the obtained heterocyclic compounds is confirmed by PMR and IR absorption spectra.
cyclohydration, monopropargyl esters, heterocyclization, butanediol, dioxane, t-BuOH, NaOH, alcohol, acetylene ethers, hydration reaction, acrolein
Введение
В настоящее время значительный интерес в области химии приобрели исследования кислородсодержащих производных ацетилена. Из простых эфиров, содержащих тройную углерод-углеродную связь, наиболее подробно изучены этиниловые и пропаргиловые эфиры одноатомных спиртов и фенолов, а также алк(ар)ариловые эфиры ацетиленовых гликолей. Алкиниловые (особенно пропаргиловые) моно- и диэфиры многоатомных спиртов изучены недостаточно.
Монопропаргиловые эфиры гликолей (I, II) получают в условиях метода конденсации пропаргилового спирта с соответствующими гликолями [1, 2]. Ацетиленовые эфиры гликолей в условиях кислотно-каталитической гидратации обычно образуют соответствующие кетооксиэфиры. Монопропаргиловый эфир 2,3-бутандиола (I) подвергается необычным превращениям в условиях реакции гидратации.
Экспериментальная часть
Инфракрасные спектры веществ в микрослое сняты на приборе UR-10, спектры протонного магнитного резонанса (ПМР) записаны на спектрометре «Вариан T-60». Циклогидратация в кислой среде. 2,5,6-триметил-2-окси-1,4-диоксан (III)
К нагретому до 50 °С и перемешиваемому раствору 1,25 г красной HgO и 2 мл H2SO4, разбавленному 48 мл воды, в течение 30 минут добавляли 12,8 г (0,1 моль) моноэфирного 2,3-бутандиола (I).
Смесь нагревали до 60 °С в течение 2 часов, охлаждали и затем экстрагировали эфиром. Эфирные вытяжки промывали насыщенным раствором Na2SO4.
Выделено 7 г (48 %) вещества с температурой кипения 56–57 °С (2 мм рт.ст.),
Найдено: С – 59,73 %; H – 9,71 %. Вычислено С – 59,58 %, H – 9,58 %.
ИК-спектр: OH – 3 450 см–1; СH3 – 1 450 и 1 385 см–1; С–О–С – 1 100 и 1 170 см–1.
Спектр ПМР («Вариан Т-60»): СH3, 3H – 1,0; СH3, 3H – 1,1; 2-СH3, 3H – 1,2; протоны кольца, 4H – 3,87; OH, 1H – 4,0.
Найдено: С – 57,58 %; H – 9,60 %. Вычислено: С – 57,51 %; H – 9,65 %.
Основная каталитическая внутримолекулярная гетероциклизация. 4,5-диметил-2-винил-1,3-диоксолан (IV) и 2,5,6-триметил-1,4-диоксен (V)
Смесь из 8 г (0,6 моль) монопропаргилового эфира 2,3-бутандиола (II) и 3,2 г едкого калия нагревали при 50 °С в вакууме (38 мм) в течение 30 минут, затем подвергали двукратной перегонке.
Выделено 4,2 г (52 %) смеси изомеров (IV, V) с температурой кипения 65–68 °С (38 мм),
Найдено: С – 65,42 %; Н – 9,31 %. С7Н12О2. Вычислено: С – 65,59 %; Н – 9,44 %.
Спектры поглощения веществ ПМР и ИК доказывают (IV, V).
ИК-спектры: СН=СН2 – 1 695 и 1 662 см–1; –982 и 3 100 см–1.
4-метил-2-винил-1,3-диоксан (IV)
Нагретую до 80 °С смесь из 19 г (0,17 моль) t-BuOK, 150 мл t-BuOН и 9,8 г (0,077 моль) (I) перемешивали в течение 10 часов.
После охлаждения к смеси добавляли 150 мл эфира и 250 мл воды. Эфирную фазу отделяли, водную экстрагировали эфиром.
В дальнейшем эфирные фазы объединяли, промывали насыщенным раствором NaСl и сушили Na2SO4. После удаления растворителя перегонкой в вакууме выделено 58 % вещества с температурой кипения 66–68 °С (39 мм),
Найдено: С – 65,72 %; Н – 9,28. С7Н12О2. Вычислено: С – 65,59 %; Н – 9,44 %.
ИК-спектры: СН=СН2 – 1 645, 3 096 и 3 035 см–1; С–О–С–О–С – 1 060–1170 см–1.
3,5-диметил-1,4-тетрагидродиоксепин (VII) в смеси с диоксаном (VI)
К нагретой до 150 °С и интенсивно перемешиваемой смеси из 6 г порошкообразного NaOH и 100 мл ДМСО быстро добавляли 12,8 г (0,1 моль) (I).
Перемешивание продолжали 15 минут, затем смесь охлаждали и добавляли 100 мл воды, многократно экстрагировали эфиром и сушили Na2SO4. После удаления растворителя перегонкой в вакууме выделено 6,6 г (52 %) смеси веществ (VI, VII) с температурой кипения 64–68 °С (40 мм),
Найдено: С – 65,84 %; Н – 9,22 %. С7Н12О2. Вычислено: С – 65,59 %; Н – 9,44 %.
ИК-спектры: >С = СН2 – 1 672 и 810 см–1; СН = СН2 – 1 645, 3 096 и 3 040 см–1.
Результаты и их обсуждение
В исследовании установлено, что в условиях реакции гидратации процесс сопровождается циклизацией с образованием 2,5,6-триметил-2-окси-1,4-диоксана (III) (рис. 1).
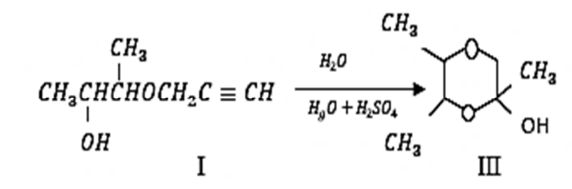
Рис. 1. Реакция циклизации монопропаргилового эфира 2,3-бутандиола (I)
Fig. 1. Cyclization reaction of 2,3-butanediol(I) monopropargyl ether
Строение продукта реакции доказано методом спектроскопии ПМР (рис. 2).
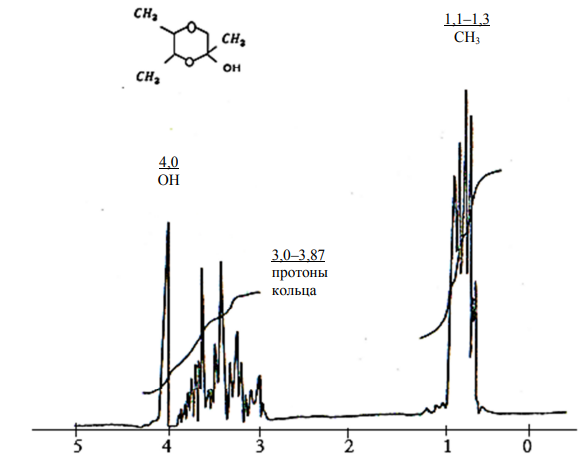
Рис. 2. Спектр ПМР 2,5,6-триметил-2-окси-1,4-диоксана (III)
Fig. 2. The PMR spectrum of 2,5,6-trimethyl-2-oxy-1,4-dioxane (III)
Используя склонность пропаргильных соединений к изменению в основной среде [3, 4], была изучена возможность превращения монопропаргиловых эфиров 2,3- и 1,3-бутандиолов (I, II) в кислородсодержащие гетероциклы. Установлено, что монопропаргиловый эфир 2,3-бутандиола (I) при нагревании в вакууме с КОН превращается не в индивидуальный продукт, а в смесь 4,5-диметил-2-винил-1,3-диоксолана (IV) и 3,5,6-триметил-1,4-диоксена (V). Идентификация последних не представляла трудностей после того, как независимым путем был синтезирован в индивидуальном виде пятичленный диоксолан (конденсацией 2,3-бутандиола с акролеином) (рис. 3).
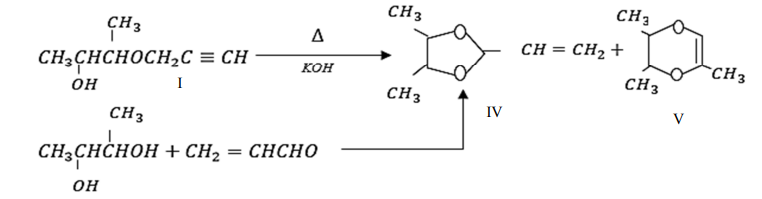
Рис. 3. Конденсация 2,3-бутандиола с акролеином
Fig. 3. Condensation of 2,3-butanediol with acrolein
Согласно данным газожидкостной хроматографии, соотношение образующихся соединений IV : V в смеси составляет 62 : 38 %. Строение синтезированных соединений (IV, V) подтверждено спектрами ПМР и ИК-поглощения (рис. 4).
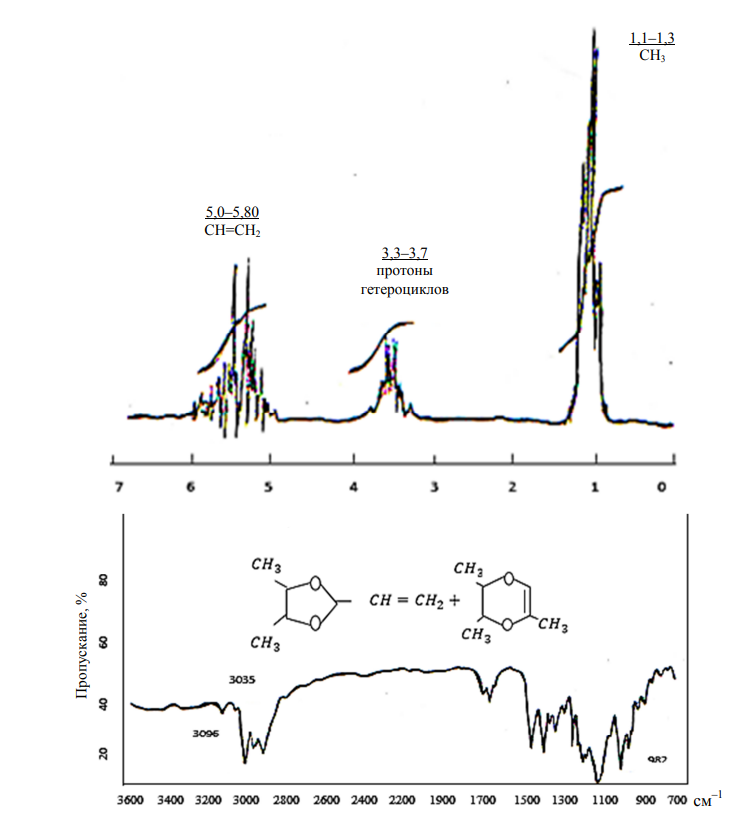
Рис. 4. Спектры ПМР и ИК-поглощения гетероциклов 4,5-диметил-2-винил-1,3-диоксолана (IV) и 3,5,6-триметил-1,4-диоксена (V)
Fig. 4. PMR and IR absorption spectra of 4,5-dimethyl-2-vinyl-1,3-dioxolan (IV) and 3,5,6-trimethyl-1,4-dioxene (V) heterocycles
Направление основной каталитической внутримолекулярной гетероциклизации монопропаргилового эфира 1,3-бутандиола (II) определяется силой основания и природой растворителя.
В присутствии t-ВuOK циклизация в t-BuOH протекает в сторону образования индивидуального 4-метил-2-винил-1,3-диоксана (VI), в то время как при катализе NaOH в реакции дегидрохлорирования наряду с последним образуется 3,5-диметил-1,4-тетрагидродиоксепин (VII) в количестве 12 % (по данным ГЖХ) [5–8].
Винилзамещенный 1,3-диоксан (VI) был получен в индивидуальном виде встречным синтезом путем конденсации 1,3-бутандиола с акролеином (рис. 5).
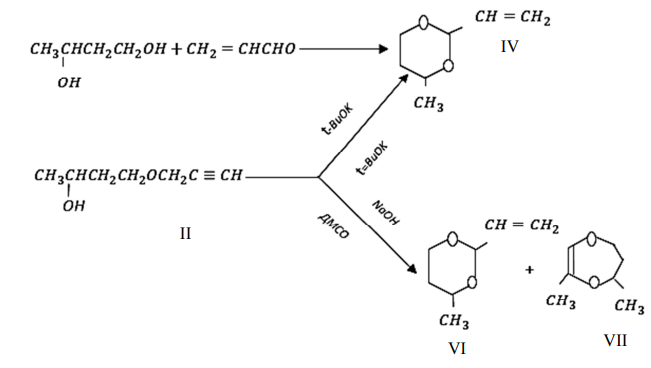
Рис. 5. Встречный синтез путем конденсации 1,3-бутандиола с акролеином
Fig. 5. Counter synthesis by condensation of 1,3-butanediol with acrolein
Строение полученных гетероциклических соединений подтверждено спектрами ПМР и ИК-поглощения (рис. 6, 7).
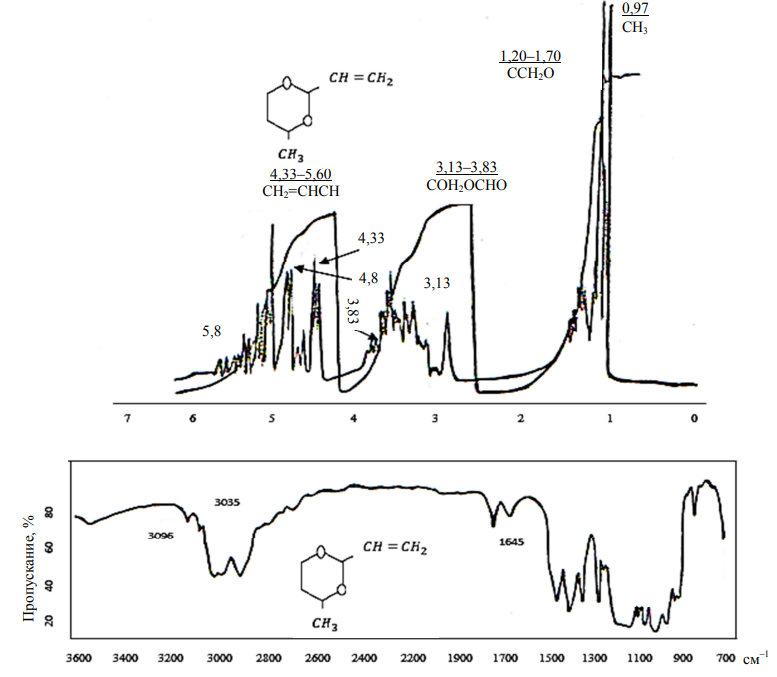
Рис. 6. Спектры ПМР и ИК-поглощения 4-метил-2-винил-1,3-диоксана (VI)
Fig. 6. PMR and IR absorption spectra of 4-methyl-2-vinyl-1,3-dioxane (VI)
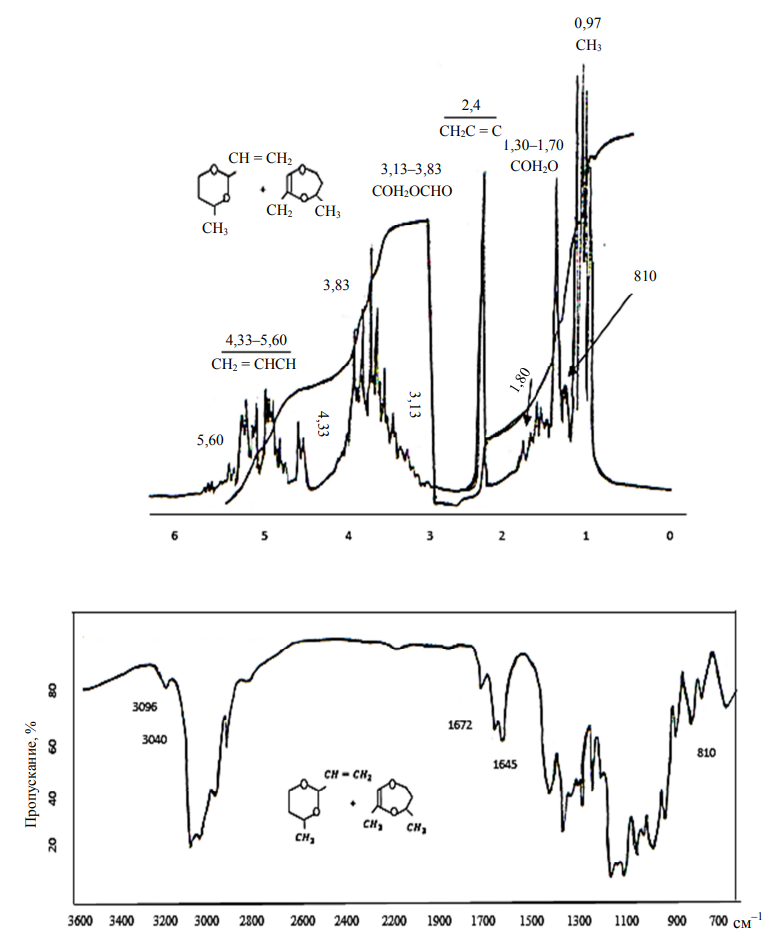
Рис. 7. Спектры ПМР и ИК-поглощения смеси гетероциклов 4-метил-2-винил-1,3-диоксана (VI)
и 3,5-диметил-1,4-тетрагидродиоксепина (VII)
Fig. 7. PMR and IR absorption spectra of a mixture of 4-methyl-2-vinyl-1,3-dioxane (VI)
and 3,5-dimethyl-1,4-tetrahydrodioxepine (VII)heterocycles
Выводы
Встречные синтезы диоксолана (IV) и диоксана (V) осуществляли конденсацией 2,3- и 1,3-бутандиолов с акролеином по методу [4]. Были получены:
1) 4,5-диметил-2-винил-1,3-диоксан (IV);
2) 4-метил-2-винил-1,3-диоксан (V).
Результаты исследования свидетельствуют о том,
что изученные эфиры с тройной связью интересны в теоретическом и практическом отношении.
Ацетиленовые эфиры зарекомендовали себя весьма ценными веществами, используемыми в различных областях органического синтеза и проявляющими интересные свойства прикладного характера.
1. Schmidt E. Yu., Bidusenko I. A., Zorina N. V. et al. Consecutive reactions of dialkile thynyl carbonyls with acetylene in super base KOH/DMSO suspension. Mendeleev Commun, 2012, vol. 22, pp. 132-133. DOIhttps://doi.org/10.1016/j.mencom.2012.05.005.
2. Bidusenko I. A., Zorina N. V. Ivanovo E. V. New chemistry of acetylene alcohols. abstract report of the All-Russian Youth Scientific Conference. Actual problems of organic chemistry. Novosibirsk, 2012. P. 11.
3. Trofimov B. A., Schmidt E. Yu. Skitaltseva E. V., Bidusenko I. A., Zorina N. V. Base catalyzed inflation of tertiary propargylic alcohols with acetylene; a first examples. Mendeleev Commun, 2012, vol. 22, pp. 62-63.
4. Schmidt E. Yu., Bidusenko I. A., Protsuk N. I, Ush-akov I. A., Trotimov B. A. Superbase‐Promoted Selective Cascade Cyclization Reaction of 1,5‐Diketones with Acetylenes to Methylene‐6,8‐dioxabicyclo[3.2.1]octanes. European Journal of Organic Chemistry, 2013, vol. 2013, iss. 12, p. 2453. DOIhttps://doi.org/10.1002/ejoc.201201700.
5. Karaev S. F., Movsumzade M. M., Agamirzoev N. A. O produktah kondensacii cropargilovogo spirta s metilglicidilovym ehfirom v prisutstvii BF3 [About products of condensation of tsropargyl alcohol with methylglycidyl ether in the presence of BF3]. Uchenye zapiski AzINEFTEHIM, 1972, no. 3, pp. 69-72.
6. Bottini A. T., Corson F. R., Bother E. F. Base-Jndused Cyclization Reaction of Proparqiloxyethanol and the 2-Haloallyoxyethanols. The Journal of Organic Chemistry, 1965, vol. 30, pp. 2988-2993.
7. Bottini A. T., Bötner E. F. Base-Jndused Cyclization Reaction of Proparqiloxyethanols. The Journal of Organic Chemistry, 1966, vol. 31, no. 1, pp. 389-391.
8. Fischer R. F. Smith C. W. Cyclic Acrolith Acetyls. The Journal of Organic Chemistry, 1959, vol. 25, no. 1, pp. 319-324.










